In der Studie waren im Verhältnis 1:1 330 Patienten mit mäßig bis hoch aktiver, akuter de-novo oder rezidivierender AAV eingeschlossen und für 52 Wochen (zur Remissionsinduktion bzw.- erhaltung) in Kombination mit entweder Cyclophosphamid (12 Wochen oral oder i.v.) oder Rituximab (4 Wochen i.v.), sowie nachfolgend Azathioprin auf Avacopan 2x 30 mg/Tag oder Prednison 60 mg/Tag mit Tapering auf null binnen 20 Wochen randomisiert worden. Primäre Endpunkte waren einerseits eine Remission in Woche 26 und andererseits eine anhaltende Remission in Woche 52 gemäß einem Birmingham Vasculitis Activity Score (BVAS) =0 und keine Glukokortikoid (GK)-Therapie für ≥4 Wochen.
Den primären Endpunkt Remission in Woche 26 erreichten 72,3 vs. 71,0 % der Patienten unter Avacopan gegenüber Prednison (p<0,0001 für Nicht-Unterlegenheit; p=0,2387 für Überlegenheit). Den primären Endpunkt anhaltende Remission in Woche 52 erreichten 65,7 vs. 54,9 % der Patienten unter Avacopan und Prednison (p<0,0001 für Nicht-Unterlegenheit; p=0,0066 für Überlegenheit). Nach erreichter Remission (BVAS =0) war die Zeit bis zu einem Rezidiv unter Avacopan signifikant länger als unter Prednison (p=0,0091; Hazard ratio, HR 0,46). Die Effektivität von Avacopan war vergleichbar in verschiedenen Subgruppen (de-novo vs. Rezidiv, PR3- vs. MPO-ANCA, GPA vs. MPA, Cyclophosphamid vs. Rituximab und Männer vs. Frauen).
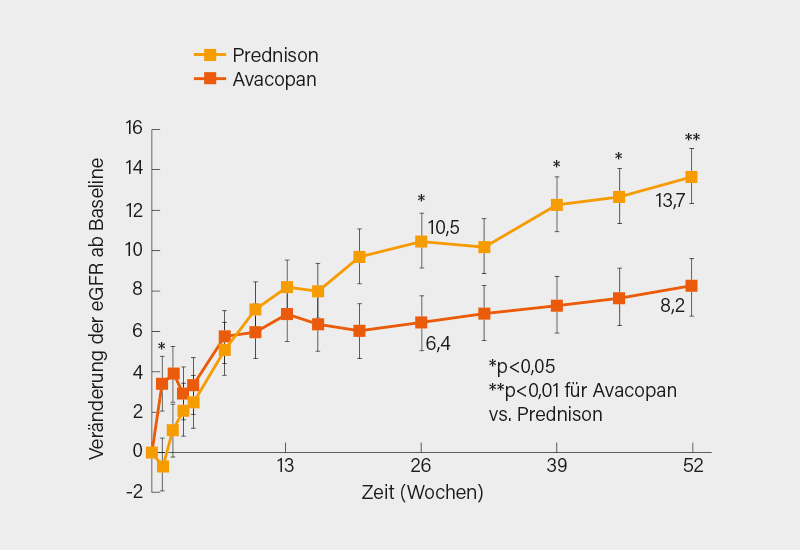
Nun zur renalen Funktion, die – als sekundärer Enpunkt – an der eGFR und dem Albumin-Kreatinin-Quotienten festgemacht wurde. In der Subgruppe mit renaler Vaskulitis zu Baseline zeigte sich im Avacopan-Arm ein gegenüber Prednison signifikant größerer Anstieg der eGFR (7,3 vs. 4,1 ml/min/1,73 m2; p=0,029) mit der größten Differenz bei Teilnehmern mit einer Baseline-eGFR <30 ml/min/1,73 m2 (Abb.). Zudem zeigte sich eine raschere Reduktion der Albuminurie unter Avacopan versus Prednison nach 4 Wochen (-40 %), nach 52 Wochen war die Gesamtreduktion in beiden Armen vergleichbar. Vorteile von Avacopan waren auch im Sicherheitsprofil ersichtlich (166 vs. 116 schwere unerwünschte Ereignisse und 31 vs. 25 schwere Infektionen). Zusätzlich zum häufigeren Erreichen einer (anhaltenden) Remission wurde mit Avacopan eine größere Verbesserung der Nierenfunktion gegenüber der GK-Standardtherapie erreicht. Gerade auch AAV-Patienten mit ausgeprägter Nierenbeteiligung könnten somit künftig von dem C5a-Rezeptorinhibitor profitieren. (1)
Kurz und kompakt
Nur kurz eingegangen sei auf das von Rona Smith, Cambridge (Großbritannien), vorgestellte 48-Wochen-Follow-up der internationalen, randomisierten, kontrollierten RITAZAREM-Studie, in der 170 AAV-Patienten mit rezidivierender Erkrankung nach Remissionsinduktion mit Rituximab im Anschluss auf eine Erhaltungstherapie mit Rituximab oder Azathioprin randomisiert wurden. Der nach 24 Monaten evidente Vorteil von Rituximab bezüglich des Rezidivrisikos (13 vs. 38 %) setzte sich im Wesentlichen auch im weiteren Vorlauf fort. (2)
Quellen:
1 Arthritis Rheumatol 2020; 72(Suppl. 10): Abstr. 0432
2 Arthritis Rheumatol 2020; 72(Suppl. 10): Abstr. 2052