Viel Interesse rief eine von David A. Katz, Portland (USA), und internationalen Kollegen (mit viel deutscher Beteiligung) vorgestellte Pilotstudie zum Einsatz des 11b-Hydroxysteroid-Dehydrogenase Typ 1 (HSD-1)-Inhibitors Clofutriben hervor, die zum Ziel hatte, bei 53 PMR-Patienten in Remission oder niedriger Krankheitsaktivität unter 10 mg/Tag Prednisolon ein darunter verbessertes Nutzen-Risiko-Profil von GK nachzuweisen. Diese wurden ohne Dosisreduktion 4 Wochen weiter mit Prednisolon behandelt, erhielten dann aber Clofutriben 6 mg/Tag für 2 Wochen nach Placebo für 2 Wochen. In konsekutiven Kohorten wurde eine Gesamtdosis von 10, 15, 20 oder 30 mg/Tag Prednisolon mit Clofutriben verabreicht.
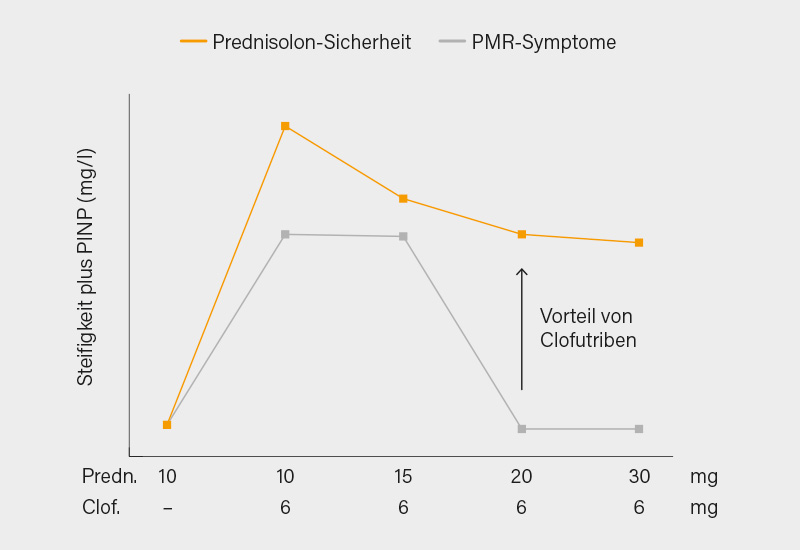
5 von 13 Patienten, die Prednisolon 10 mg/Tag plus Clofutriben erhielten, erlitten ein Rezidiv. Es traten keine Rezidive auf, wenn höhere Prednisolon-Dosen mit Clofutriben verabreicht wurden oder während Prednisolon 10 mg/Tag plus Placebo. Teilnehmer berichteten nur über schwerere Symptome und körperliche Einschränkungen, wenn Prednisolon 10 oder 15 mg/Tag, aber nicht, wenn Prednisolon 20 oder 30 mg/Tag mit Clofutriben verabreicht wurde. Entzündungsbiomarker folgten einem ähnlichen Muster. Über alle Prednisolon-Dosen hinweg milderte die gemeinsame Verabreichung von Clofutriben GK-bedingte Nebenwirkungen auf Biomarker der Knochenbildung und -resorption, Lipidstoffwechsel, Hyperkoagulabilität sowie die kardiovaskuläre und adrenale Funktion. Die Kurzzeitstudie zeigte somit, dass Clofutriben in Kombination mit Prednisolon die GK-assoziierte Toxizität mildert und gleichzeitig deren entzündungshemmenden Eigenschaften aufrechterhält (Abb.), ein günstigeres Nutzen-Risiko-Profil dieser Kombination suggerierend – Langzeitdaten bleiben abzuwarten. (1)
Im Fokus: MTX und Secukinumab
Weiter fraglich bliebt der Nutzen von Methotrexat (MTX) zur Steroidreduktion bei PMR. Eine 52-wöchige randomisierte, doppelblinde, placebokontrollierte Studie niederländischer Rheumatologen um Aatke van der Maas, Nijmegen, lässt darauf schließen, dass höher dosiertes MTX (25 mg/Woche) zumindest bei neu diagnostizierten PMR-Patienten effektiv sein könnte. Im Verhältnis 1:1 wurden 58 Patienten auf MTX oder Placebo im Verbund mit einem 24-wöchigen GK-Tapering randomisiert. Den primären Endpunkt einer GK-freien Remission zu Woche 52, definiert als PMR-Aktivitätsscore (AS) <10 und kein GK, erreichten 80 vs. 46 % der Patienten (p=0,0042). Überdies zeigte sich eine signifikant niedrigere Rate an Rezidiven (Inzidenzraten-Verhältnis, IRR 0,62; p=0,046) sowie eine kürzere Zeit bis zur GK-freien Remission (28 vs. 39 Wochen; p=0,013). In anderen sekundären Endpunkten und bei Nebenwirkungen fanden sich keine signifikanten Unterschiede. Für selektierte PMR-Patienten könnte MTX hilfreich sein, weitere Daten hierzu wären aber wünschenswert. (2)
Zum bei PMR zugelassenen Sarilumab könnte sich perspektivisch der Interleukin-17A-Inhibitor Secukinumab gesellen, der in der Phase-II-TiTAIN bei RZA überzeugt hatte und derzeit bei RZA und PMR in Phase-III-Studien geprüft wird. Eine von Nils Venhoff, Freiburg, und Kollegen vorgelegte Post-hoc-Analyse der TiTAIN-Studie zu einer (allerdings recht kleinen) Subgruppe vom 20 RZA-Patienten mit PMR lässt auch in dieser Indikation auf gute Daten hoffen. Nur bei 8,3 vs. 50 % der Teilnehmer in der Placebo-Gruppe wurden nach Initiierung von Secukinumab PMR-Symptome festgestellt. (3)
Quellen:
1 Ann Rheum Dis 2025; 84 (Suppl 1): 51 (OP0058)
2 Ann Rheum Dis 2025; 84 (Suppl 1): 56 (OP0064)
3 Ann Rheum Dis 2025; 84 (Suppl 1): 54 (OP0062)