Deutsche Rheumatologen um Nils Venhoff, Freiburg, untersuchten in der randomisierten, doppelblinden, placebokontrollierten Phase-II-Parallelgruppenstudie TitAIN den IL-17A-Inhibitor Secukinumab. In die Proof-of-concept-Studie gingen 52 Biologika-naive Patienten in einem Alter ≥50 Jahre mit de-novo (80 %; diagnostiziert ≤6 Wochen vor Baseline) oder rezidivierender (20 %; diagnostiziert >6 Wochen vor Baseline) RZA ein. Diese wurden im Verhältnis 1:1 auf Secukinumab 300 mg (n=27) oder Placebo (n=25) zu Beginn wöchentlich (5 Dosen) und danach alle 4 Wochen bis Woche 48 (letzte Dosis) randomisiert – kombiniert mit einem jeweils 26-wöchigen GK-Tapering ab Baseline. Primärer Endpunkt war der Anteil von Patienten in anhaltender Remission bis Woche 28. Wichtige sekundäre Endpunkte waren der Anteil von Patienten mit anhaltender Remission bis Woche 52 sowie die Zeit bis zum ersten Rezidiv.
Secukinumab überzeugt in Phase-II-Studie
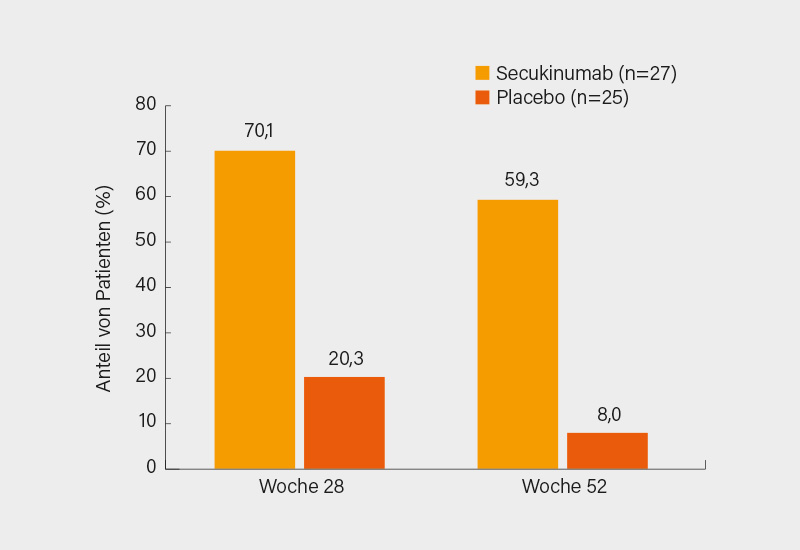
Unter Secukinumab schlossen 81,5 % der Patienten die Studie ab, unter Placebo 60,0 %. Der Anteil von RZA-Patienten in einer anhaltenden Remission bis Woche 28 war unter Secukinumab im Vergleich zu Placebo höher mit 70,1 vs. 20,3 % (Odds ratio, OR 9,31), gleiches galt für den sekundären Endpunkt, das Erreichen einer anhaltenden Remission bis Woche 52 mit 59,3 vs. 8,0 % (Abb.). Die mediane Zeit bis zum ersten Rezidiv wurde für Secukinumab nicht erreicht und betrug 197 Tage mit Placebo. Unerwünschte Ereignisse (UE) waren ähnlich verteilt, schwere UE waren unter Secukinumab sogar seltener (100 vs. 96 % bzw. 22 vs. 44 %). In beiden Gruppen gab es je einen Todesfall (nicht therapieassoziiert). Es wurden keine neuen Sicherheitssignale verzeichnet. Secukinumab führte somit häufiger zu einer anhaltenden Remission und längeren Zeit bis zum ersten Rezidiv über 52 Wochen, sodass dessen Weiterentwicklung bei RZA wohl vielversprechend wäre. (1)
Tocilizumab plus 8 Wochen Prednison effektiv
Nachdem eine zu kurze Hochdosis-GK-Therapie (für 3-4 Tage) plus Tocilizumab nicht zu ausreichend hohen Remissionsraten führte, untersuchten Sebastian Unizony, Boston (USA), und Kollegen, ob sich die GK-Exposition von üblicherweise 6 auf 2 Monate in Kombination mit Tocilizumab reduzieren lässt. In die prospektive, einarmige Open-label-Studie wurden 30 Patienten mit aktiver RZA (im Mittel 74 Jahre, 60 % Frauen, 57 % de-novo, bei 77 bzw. 47 % Nachweis durch TA-Biopsie oder Bildgebung, ESR 45 mm/h, CRP 48 mg/l) eingeschlossen. Als aktive RZA zählten (binnen 6 Wochen ab Baseline) therapiebedürftige kranielle oder Polymyalgia rheumatica (PMR)-Symptome. Alle Patienten erhielten s.c. Tocilizumab 162 mg/Woche sowie ein 8-wöchiges Prednison-Tapering ausgehend von 20 bis 60 mg/Tag. Primärer Endpunkt war eine anhaltende Prednison-freie Remission, definiert als kein Rezidiv (erneute Symptome, die unabhängig von ESR/CRP eine Intensivierung der Therapie erfordern) ab der Remissionsinduktion bis Woche 52 bei protokollgerechtem Prednison-Tapering.
Alle Patienten gelangten in eine Remission binnen 4 Wochen, den primären Endpunkt erreichten 77 %. Die mittlere kumulative GK-Dosis bei diesen 23 Patienten betrug 1.052 mg. Nach im Mittel 16 Wochen war es bei 7 Patienten (23 %) zu einem Rezidiv gekommen – in allen Fällen nach abgeschlossenem Prednison-Tapering, 6 davon erhielten ein 2. Prednison-Tapering über 8 Wochen, 4 davon erreichten eine anhaltende Remission. Die mittlere kumulative GK-Dosis bei den 7 Patienten mit Rezidiv betrug 1.883 mg. Bei 13 Teilnehmern kam es zu einem schweren UE, nicht aber zu einem permanenten Visusverlust. Die Daten deuten an, dass die Kombination aus wöchentlicher Tocilizumab-Gabe für 12 Monate mit einem 8-wöchigen Prednison-Tapering (also so lange, bis der volle Wirkspiegel der IL-6-Inhibition erreicht ist) effektiv genug für eine andauernde Remission bei vielen RZA-Patienten sein könnte. Dieses Protokoll müsste jetzt in einer randomisierten, kontrollierten Studie evaluiert werden. (2)
Hoher Stellenwert des Ultraschalls bestätigt
Eine spanische Arbeitsgruppe um Elisa Fernández-Fernández, Madrid, präsentierte eine Studie, in der die Validität der EULAR-Empfehlungen zum Einsatz des Ultraschalls in der Diagnostik der RZA untersucht wurde – mit besonderem Fokus auf die farbkodierte Doppler-Sonografie (FDUS). Die Ergebnisse zeigen, dass die Kombination der Resultate eines Vortestwahrscheinlichkeits-Scores mit dem FDUS eine akkurate RZA-Diagnose erlaubt mit einer Fehlklassifikation in nur 2 % der Fälle. Selbst ein negativer FDUS bei Patienten mit intermediärem Risiko zeigte eine starke Assoziation mit einer negativen Diagnose – was die Schlussfolgerungen der EULAR-Leitlinie zur US-Diagnostik stützt. (3) Spannend war das Abstract einer internationalen Gruppe um Eugenio de Miguel, gleichfalls Madrid (Spanien), das sich mit den eng verwandten Entitäten PMR und RZA beschäftigte. Eine PMR tritt bei ca. 50 % der RZA-Patienten auf. Umgekehrt wurde jetzt bei 258 neu diagnostizierten PMR-Patienten mittels vaskulärem US untersucht, wie häufig sich eine subklinische RZA findet. Es zeigte sich, dass bei einem Fünftel der PMR-Patienten ohne Zeichen und Symptomen einer RZA im US mit der Diagnose einer RZA vereinbare Befunde vorlagen. Bei 24,3 % war nur die Temporalarterie betroffen, bei 65,8 % zeigte sich eine extrakraniale Beteiligung und bei 9,8 % eine Mischform. (4)
Quellen:
1 Ann Rheum Dis 2022; 81(Suppl 1): 121-122 (Abstr. OP0182)
2 Ann Rheum Dis 2022; 81(Suppl 1): 123 (Abstr. OP0185)
3 Ann Rheum Dis 2022; 81(Suppl 1): 122 (Abstr. OP0183)
4 Ann Rheum Dis 2022; 81(Suppl 1): 122-123 (Abstr. OP0184)