INTERESSANTE ALLGEMEINE THEMEN
Was bereits beim letzten EULAR-Kongress in einer niederländischen, inzwischen auch vollpublizierten Studie thematisiert worden war (1), wurde jetzt in Chicago in zwei weiteren Untersuchungen aufgegriffen: Die in unseren Therapieblättern vorgegebenen Laborkontrollen der DMARD-Therapie sind offenkundig viel zu umfangreich. In einer retrospektiven texanischen Analyse bei 3.821 Patienten unter Methotrexat (MTX) wurden bei Vergleich von Kontrollen alle sechs vs. alle drei Monate keine Unterschiede bezüglich der Auffindung von (generell sehr seltenen) pathologischen Ergebnissen gefunden. (2) Dies wurde in einer weiteren Kohortenstudie mit 2.606 Patienten unter MTX bestätigt (3), in der generell nur bei 2 % der Kontrollen Abweichungen mit Konsequenzen (2/3 Therapieende, 1/3 Dosisreduzierung) festgestellt wurden. Dass vorgegebene Pläne für Kontrollen zu einem eigentlich unvertretbaren Aufwand führen, wurde hier dadurch unterstrichen, dass diese Kontrollen 4.546 zusätzliche Blutentnahmen, 84 zusätzliche Visiten, 104 bildgebende Untersuchungen und sogar 18 bioptische Abklärungen nach sich zogen.
Wie intensiv nutzen Rheumapatienten das Internet? Dieser Frage ging eine Querschnittsstudie des Rheumazentrums Rhein-Ruhr mit 705 befragten Patienten (darunter 53,8 % mit RA) nach. (4) Insgesamt 78,3 % nutzten das Internet (zu 80 % via Smartphone), darunter Patienten mit früher Erkrankung signifikant häufiger und fast 20 % mehrfach wöchentlich. Für eine Mehrbelastung des Rheumatologen dadurch spricht, dass 83,7 % wegen der gelesenen Inhalte dann in der Praxis nachfragen. Die meistgefragten Themen waren Ernährung (84,5 %), Therapie (83,3 %), Krankheitssymptome (81,6 %), Wirksamkeit der Therapie (80,6 %) und Bedeutung der physikalischen Therapie (79,4 %).
ALLGEMEINES ZUR RHEUMATOIDEN ARTHRITIS
Zu den für Rheumapatienten relevantesten Problemen zählt die Fatigue, für die zugleich leider oft nur limitierte Behandlungsmöglichkeiten bestehen, Besserung also nur partiell zu erwarten ist. In einer spanischen Untersuchung bei 246 RA-Patienten gelang es immerhin bei 102, eine komplette Remission zu erreichen. (5) Gleichwohl litten 27,4 % der Patienten an persistierenden Fatigue-Beschwerden mit relevantem Ausmaß. Frauen, Raucher und Patienten mit anamnestischer Depression waren bevorzugt betroffen. Leider sind Behandlungskonzepte für Fatigue dünn gesät, neuere Studien legen nahe, dass Verhaltenstherapie und insbesondere hochintensive Übungstherapie (6) erfolgreich sind. Der Vollständigkeit halber ist zu ergänzen, dass für das Selbstmanagement einige verschreibungsfähige Fatigue-Apps (z. B. Elevida, Untire, Fimo Health App ME/CFS) zur Verfügung stehen, die aber leider nicht explizit für Rheumapatienten entwickelt wurden.
Das thromboembolische Risiko ist im RA-Krankengut bekanntermaßen signifikant erhöht. In einer bevölkerungsbasierten Studie der RA-Langzeitkohorte der Mayo-Klinik mit je 1.409 RA-Patienten und gematchten Kontrollen wurde jetzt für RA eine signifikante Hazard Ratio (HR) von 2,26 für tiefe Beinvenenthrombosen und 1,61 für Lungenembolie ermittelt. (7) Signifikant erhöht zeigte sich auch die Mortalität nach thromboembolischen Ereignissen (HR 1,52). Während Remission mit einer signifikanten Risikoreduzierung verbunden ist, erwiesen sich (wie zu vermuten) Alter, Adipositas, Rauchen und schwere Krankheitsausprägung als relevante Risikofaktoren. Auch Vorhofflimmern tritt bei RA gehäuft auf: In einer koreanischen Untersuchung zeigte sich eine HR von 1,55. (8) Seropositive Patienten boten hier ein deutlich höheres Risiko als seronegative. In diesem Zusammenhang ist interessant und innovativ, dass in zwei Beiträgen auf eine Risikoerhöhung für Rhythmusstörungen durch Interleukin-6-Rezeptorinhibitoren (IL-6Ri), insbesondere Tocilizumab, hingewiesen wurde. (9, 10) Dies betraf vor allem Tachykardien und Bradykardien, aber auch eine Risikoerhöhung für Vorhofflimmern.
Als absolutes „Modethema“ erweist sich jetzt auch in der Rheumatologie der Einsatz und Nutzen von Glucagon-like Peptide (GLP)-1-Rezeptoragonisten, er wurde auch in Chicago mehrfach thematisiert. Speziell für die RA wurde eine retrospektive Kohortenstudie mit je 2.698 gematchten RA-Patienten mit und ohne diese Begleittherapie vorgestellt, die Patienten waren adipös, aber ohne Typ-2-Diabetes. (11) Die Therapie führte zu einer signifikanten Reduktion von Gesamtmortalität, schweren kardialen Ereignissen und Herzinsuffizienz, numerisch auch zur Verringerung der Rate an Herzinfarkten und Schlaganfällen. In anderen Beiträgen wurden positive Ergebnisse auch bei PsA und Arthrose gezeigt.
INTERSTITIELLE LUNGENERKRANKUNG IM RAHMEN DER RA
Weiterhin steht die interstitielle Lungenerkrankung (ILD) als Manifestation der RA wegen ihrer schlechten Prognose im Mittelpunkt des Interesses, sie wurde auch in Chicago vieldiskutiert. Inzidenz und Prävalenz der ILD bei „Connective Tissue Diseases“ (CTD) insgesamt wurden in einer Untersuchung aus zwei US-Datenbanken ermittelt. (12) Es bestätigte sich, dass die Prävalenz innerhalb dieser Gruppe bei RA bei weitem am höchsten ist, gefolgt mit Abstand von der SSc. Anhand einer Hochrechnung kann man in Deutschland von rund 35.000 CTD-ILD-Patienten ausgehen. Die Suche nach Biomarkern für ein erhöhtes ILD-Risiko bei RA geht mit großer Anstrengung voran – in einer Querschnittsanalyse mit 2.737 RA-Patienten, darunter 124 mit RA-ILD, erwies sich der Growth Differentiation Factor (GDF)-15, ein Mitglied der Transforming GF (TGF)-b-Familie, als unabhängig assoziiert sowohl mit prävalenter wie auch inzidenter RA-ILD. (13)
In einer spanischen Untersuchung mit 270 RA-Patienten, darunter 21,5 % mit ILD, wurde nach der Wertigkeit von Thorax-Röntgen und Lungenfunktion – beide in vielen Leitlinien noch als nützlich vorgegeben – für das RA-ILD-Screening gesehen. (14) Sensitivität und Spezifität beider Untersuchungen erwiesen sich als unzureichend, für gute Ergebnisse ist eine HRCT-Untersuchung unverzichtbar. Jedoch sind Lungenfunktionstests zumindest für Verlaufsuntersuchungen ein wichtiges Instrument. Vermehrt wird die Sonografie für die Diagnostik der ILD eingesetzt, hat aber – abgesehen von der erforderlichen hohen Expertise – bisher noch nicht den Stellenwert des HRCT. In einer chinesischen Studie mit 146 CTD-ILD-Patienten ergab sich für die Unterscheidung zwischen präklinischer, limitierter und extensiver ILD für die Methode immerhin eine Sensitivität von 95,7 bzw. 89,7 % und Spezifität von 83,3 bzw. 73,8 %, außerdem eine recht gute Korrelation zu den Ergebnissen der gleichzeitig durchgeführten HRCT. (15)
Mehrere Untersuchungen hatten den Zusammenhang zwischen RA-ILD und Komorbiditäten zum Thema. Das Risiko für schwere Infektionen unter RA-ILD und RA plus Bronchiektasie wurde in einer gematchten Kohortenstudie untersucht. (16) Das Risiko für pulmonale Infektionen war jeweils deutlich erhöht (Haupterreger Influenza, RSV, Staphylokokken und Pseudomonas), schwere Infektionen traten jedoch nur bei RA-ILD signifikant gehäuft auf (HR 1,79). Eine US-amerikanische Arbeitsgruppe ging bei 69.915 RA-Patienten der Frage nach, ob RA-ILD einen Risikofaktor für kardiovaskuläre Ereignisse darstellt. (17) Schwere kardiale Ereignisse (MACE) und Herzinsuffizienz traten in der Tat signifikant gehäuft auf.
Von besonderem Interesse sind – nicht zuletzt wegen der nach wie vor ungünstigen Prognose der Erkrankung – die optimale Wahl der DMARD-Therapie bei RA-ILD und die Rolle antifibrotischer Therapien. In Chicago wies ein systematischer Review auf die zunehmend wichtige Rolle der Januskinase-Inhibitoren (JAKi) bei RA-ILD hin: Auf der Basis von 20 Studien konnte gezeigt werden, dass in über 80 % eine Stabilisierung des HRCT-Befundes und in über eine 70 % Stabilisierung der Lungenfunktionstests mit dieser Therapie erreicht werden kann. (18) Einzeluntersuchungen belegten darüber hinaus die Effektivität von Baricitinib und Upadacitinib. (19, 20) Seitens der Antifibrotika ist in den USA soeben Nerandomilast als effektive und vermutlich im Vergleich zum bisher eingesetzten Nintedanib besser verträgliche Substanz zugelassen worden. In Chicago wurden Wirksamkeit und Sicherheit dieser Substanz bei CTD-ILD anhand der Daten der FIBRONEER-Studie vorgestellt, die den potenziellen Nutzen dieser Therapie unterstreicht. (21)
GLUKOKORTIKOIDE UND KONVENTIONELLE DMARDS
Eine Untersuchung der Charité mit Auswertung von fünf RCTs und 1.112 RA-Patienten unter zweijähriger Glukokortikoid (GK)-Therapie mit den Zielgrößen Knochendichte (BMD) und Frakturen konnte zeigen, dass die BMD nur an der Lendenwirbelsäule unter GK mehr als bei den Kontrollen abnahm. Insgesamt kam es zu 24 Frakturen ohne Gruppenunterschied. (22)
Ein überraschendes Ergebnis lieferte eine in New Mexico erfolgte Untersuchung: Kortikoid-Injektionen führten bei Patienten mit vorbestehender neuropsychiatrischer Erkrankung in 4 % zu akuten Symptomen, in erster Linie Panikattacken und vasomotorische Symptome. (23) Die Symptome klangen innerhalb von drei Tagen ab und traten bei wiederholter Injektion immer wieder auf, sie sprechen auf eine kurze Benzodiazepin-Gabe an. Die Häufigkeit GK-induzierter Hauttoxizität bei Verwendung einer höheren Startdosis (im Mittel 30 mg) wurde in Boston untersucht. (24) Es traten nicht nur in 38 % (wie bekannt) Hämatome auf, sondern in 15,5 % ein akneiformer Ausschlag und in 22 % Striae und Atrophie. Bei längerer Gabe kam es über sechs Monate zu einer kontinuierlichen Verschlechterung.
Eine spannende französische placebokontrollierte Untersuchung zur Wirksamkeit von MTX wurde als Late-Breaker noch in das Programm aufgenommen. (25) Bei oraler Gabe konnte gezeigt werden, dass durch Ballaststoff-angereicherte Kost (mittels Inulin) über 30 Tage die Wirksamkeit signifikant verbessert werden konnte: So nahm z. B. der DAS28 – bei stabiler csDMARD-Gabe – in der Verumgruppe um 1,0 ab, in der Kontrollgruppe jedoch um 0,34 zu, die Odds-Ratio (OR) für die EULAR-Response lag unter Verum bei 4,65. Begleitend wurde eine signifikante Reduzierung zirkulierender Th17-Zellen und der Th17/Treg-Ratio ermittelt. Diese Effekte waren bei anderen csDMARDs nicht zu beobachten.
In der ebenfalls in Frankreich durchgeführten METHOFRACT-Kohortenstudie wurden von 2012 bis 2024 retrospektiv 92 Fälle einer typischen, durch MTX ausgelösten Osteopathie ermittelt. (26) Betroffen waren zu 93 % postmenopausale Frauen, von denen nur rund ein Drittel dauerhaft GK einnahmen und 56 % eine Osteoporose aufwiesen, eine Frakturanamnese lag bei 22 % vor. Typische Lokalisationen waren Tibiametaphyse (88 %) und Fußknochen (49 %), in 76 % lagen multiple Lokalisationen vor. Wird eine solche Osteopathie entdeckt, sollte MTX auf keinen Fall fortgeführt werden, in solchen Fällen trat in 71 % ein baldiges Rezidiv auf.
Eine neue Metaanalyse über 10 Studien (27) verglich die Wirksamkeit und Verträglichkeit von MTX und Leflunomid – mit überraschendem Ergebnis: Bei Heranziehen des Parameters ACR70-Response und einjähriger Gabe erwies sich Leflunomid als signifikant besser wirksam (OR 0,46). Allerdings zeigte sich für MTX eine signifikant bessere Verträglichkeit (Abbruch wegen Nebenwirkungen; Risk Ratio, RR 0,71). Bis auf Mundulzerationen kamen alle Nebenwirkungen, insbesondere Diarrhöe, Alopezie und Hypertonie, unter Leflunomid signifikant häufiger vor.
BIOLOGIKA UND JAK-INHIBITOREN
Trotz der weiterhin hohen Anwendungsrate nehmen die Beiträge zur Therapie der RA mit bDMARDs von Jahr zu Jahr ab – es gibt offenkundig nicht mehr so viel Neues zu berichten. Einige spannende Neuigkeiten sind aber doch zu erwähnen. Für den First-Line-Einsatz bei RA gibt es zwar bei den meisten bDMARDs eine Zulassung, allerdings ist er in den Leitlinien nicht empfohlen und wird von deutschen Rheumatologen höchstens in Ausnahmefällen angewendet. Eine britische Studie aus der Arbeitsgruppe von Paul Emery konnte in Chicago allerdings erhebliche Vorteile für diese Variante belegen. (28) Bei Vergleich von 114 First-Line-behandelten und 228 gematchten „normal“ behandelten Patienten mit früher RA zeigte sich, dass nach fünf Jahren der Anteil von Patienten mit medikamentenfreier Remission bei First-Line-TNFi-Einsatz doppelt so hoch war wie beim Vorgehen nach Leitlinien (13 vs. 6 %). Patienten mit Einstufung als schwer behandelbare (D2T-)RA waren mit einer einzigen Ausnahme nur bei den Patienten mit leitliniengemäßem Vorgehen zu finden, die Häufigkeit lag bei 7 vs. 1 %. Das Kostenargument zugunsten eines verzögerten bDMARD-Einsatzes, wie er in Deutschland (oft in erheblichem Ausmaß) üblich ist, wirkt übrigens nicht stichhaltig. In einer weiteren paneuropäischen Untersuchung (29) konnten Daniel Aletaha und Kollegen zeigen, dass der frühe Einsatz von Adalimumab durch die Reduzierung von Kontrolluntersuchungen, Arztbesuchen und Hospitalisationen sogar Kosten einspart.
Zu zögerlich werden bDMARDs nicht nur im Verlauf der RA, sondern generell bei älteren Patienten eingesetzt, nicht zuletzt in der Meinung, dass unerwünschte Wirkungen hier häufiger sind. Die wurde in einer US-Untersuchung mit Vergleich von 1.219 LORA (Late Onset)- und 6.030 YORA (Young Onset)-Patienten erneut widerlegt (30): Das Risiko für schwere Infektion nahm zwar mit zunehmendem Alter absolut zu (wie es auch in der Normalbevölkerung zu beobachten ist), lag aber adjustiert sogar unter dem der YORA-Patienten. Tatsächlich relevante Risikofaktoren waren im Gegensatz zum Alter frühere Infektionen und eine Langzeit-GK-Therapie. Für TNFi wird seit Langem ein höheres Risiko für demyelinisierende Erkrankungen diskutiert – dies stellt zwar keine Kontraindikation dar, sollte aber zu Vorsicht führen. Wie aber sieht es bei den anderen bDMARDs aus? In einer retrospektiven Kohortenstudie wurden 51 Patienten mit demyelinisierenden Erkrankungen (meistens Multiple Sklerose, MS) unter einer Nicht-TNF-bDMARD-Therapie beobachtet (40x IL-17i, 5x IL-6Ri, 9x Abatacept, 12x Rituximab, 7x JAKi, 5x IL-23i). In keinem Fall waren Komplikationen zu beobachten, sechs Patienten erhielten ohne Probleme eine Kombination mit MS-Therapeutika. (31)
JAKi werden bei immer mehr Erkrankungen in Studien erfolgreich eingesetzt. So wurden in Chicago positive Erfahrungen u. a. für Morbus Behçet (32), Panuveitis (33), SSc (34) und SLE (35) berichtet. Vermehrt wird auch über den Erfolg von Kombinationen zwischen JAKi und bDMARDs bei therapierefraktären Patienten berichtet. Eine belgische Arbeitsgruppe stellte eine erfolgreiche Behandlung von Infliximab oder Etanercept in Kombination mit Upadacitinib oder Filgotinib bei fünf vorher refraktären Patienten vor. (36) Aus Vorsichtsgründen wurden Patienten mit schweren Infektionen oder nicht-optimiertem Impfstatus ausgeschlossen, so kam es zu guter Verträglichkeit ohne Infektionsprobleme. Im Gegensatz dazu berichtete eine spanische Arbeitsgruppe über 19 Patienten, die mit ähnlichen Kombinationen auch erfolgreich behandelt wurden, hier wurde die Therapie aber in 42 % vorzeitig beendet, in 25 % wegen Infektionen. (37) Erfreulich ist, dass sich im Programm des ACR-Kongresses keine Beiträge mehr fanden, die die auf der ORAL Surveillance-Studie beruhenden früheren Warnhinweise erneut bestätigt hätten. Die Aufregung um diese Studie und ihre Folgen scheint endgültig überwunden.
Der Einfluss von Immunsuppressiva auf die Zoster-Impfresponse wurde in einer spanischen Studie mit 157 Patienten untersucht. (38) Unter JAKi ergab sich ein deutlich verringertes humorales und zelluläres Ansprechen, dieser Effekt war hingegen unter TNFi bzw. MTX nur gering ausgeprägt. Welche praktische Bedeutung diese Ergebnisse haben (geringerer Impfschutz?), bleibt aber vorerst offen. In einer weiteren Untersuchung wurde im Übrigen gezeigt, dass unter Rituximab auch die Zoster-Impfantwort erheblich reduziert ist. (39)
VERSCHIEDENES
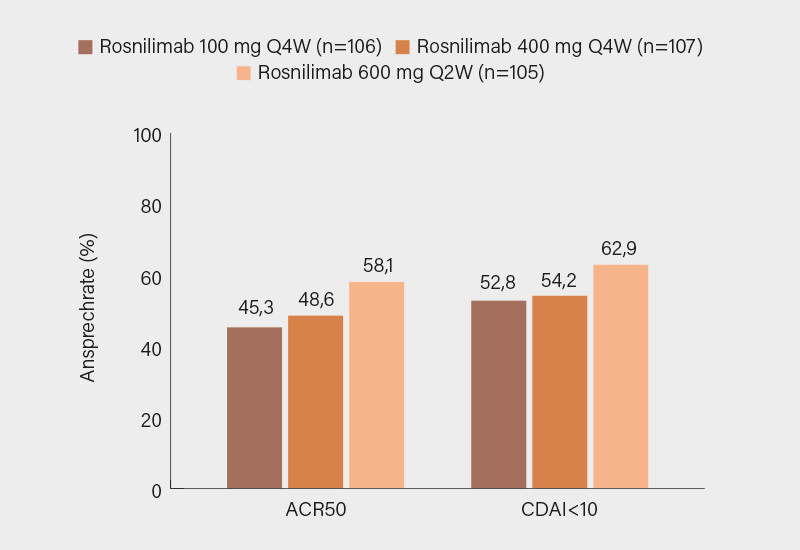
Erstmals seit einigen Jahren wurde in Chicago wieder eine Substanz vorgestellt, die einen deutlichen Fortschritt für die RA-Therapie verspricht: Rosnilimab, ein selektiv pathogene T-Lymphozyten blockierender monoklonaler Antikörper – im Late-Breaker-Sortiment aufgenommen (40) – wurde mit Ergebnissen einer Phase-IIb-Studie mit immerhin 424 Teilnehmern präsentiert. Zu den erstaunlichen und vielversprechenden Ergebnissen zählen in Woche 28 eine ACR50/70-Response von bis zu 58 bzw. 45 % und CDAI-LDA von bis zu 63 % (Abb.) – dies alles bei sehr guter Verträglichkeit.
Nach zuvor widersprüchlichen Studienergebnissen lieferten mehrere Studien Aufwind für das Therapieprinzip der Vagus-Stimulation (41, 42). Besonders vielversprechend: In einer der US-amerikanischen Studien konnte sogar placebokontrolliert gezeigt werden, dass die radiologische Progression gebremst wird. (43) Schlussendlich weckte eine indische Studie Interesse, in der placebokontrolliert bei je 70 Patienten auf MTX standardisierte ayurvedische Substanz mit Placebo verglichen wurde. (44) Die ayurvedische Kombination zeigte sich bei guter Verträglichkeit über 15 Monate in allen Parametern überlegen (ACR20/50/70-Ansprechen 90,8 vs. 70,8 %, 81,5 vs. 60 % und 36,9 vs. 27,7 %). Inwieweit sich diese positiven Erfahrungen bei einer mitteleuropäischen Patientenpopulation reproduzieren lassen, bleibt abzuwarten.
Prof. Dr. med. Klaus Krüger
Facharzt für Innere Medizin und Rheumatologie
Praxiszentrum St. Bonifatius
St.-Bonifatius-Str. 5, 81541 München
Literatur: 1 Ulijin E et al., Ann Intern Med 2025; 178(10): 1400-1408 | 2 Simko S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1370 | 3 Reed G et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2571 | 4 Andreica I et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0152 | 5 Morlà Novell RM et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0379 | 6 Bilberg A et al., Arthritis Res Ther 2025; 27(1): 176 | 7 Frechette N et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1320 |8 Kim H et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1893 | 9 Khanfar A et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0479 | 10 Mateo Faxas S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2283 | 11 Loizidis G & Summer R, Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0445 | 12 Martins D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0154 | 13 England B et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1746 | 14 Loarce J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1335 | 15 Ding J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2611 | 16 Zhang Q et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1747 | 17 Khan O et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1658 | 18 Compán O et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1321 | 19 Serrano-Combarro A et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2229 | 20 Serrano-Combarro A et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1258 | 21 Hoffmann-Vold A-M et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1662 | 22 Palmowski A et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0338 | 23 Kavosh M et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2040 | 24 Chiha T et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0792 | 25 Immediato Daien C et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB15 | 26 Robin F et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2115 |27 Pitliya A et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1347 | 28 Toyoda T et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1677 | 29 Aletaha D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2271 | 30 Lee J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1065 | 31 Azzedine D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1095 | 32 Sulu B et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0241 | 33 Barroso Garcia N et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0268 | 34 Di Donato S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1586 | 35 Mosca M et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0662 | 36 Natalucci F et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2272 | 37 Lopez Juanes N et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2042 | 38 Sieiro C et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0982 | 39 Emi Aikawa N et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2573 | 40 Graf J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB19 | 41 Valenzuela G et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1675 | 42 Tesser J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2278 | 43 Peterfy C et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2614 | 44 Priyadarshani Sethi P et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1364