SJÖGREN-ERKRANKUNG
ERSTMALS ERFOLGREICHE PHASE-III-STUDIEN VORGESTELLT
Noch gibt es für das nun in Sjögren-Erkrankung (SjD) umbenannte Sjögren-Syndrom keine eigentlich zugelassene Therapie. Aber das wird sich ab 2026 ändern. Eines der Late-Breaking Abstracts berichtete die Ergebnisse zweier Phase-III-Studien, NEPTUNUS-1 und 2, mit dem Anti-BAFF-Rezeptor-Antikörper Ianalumab. (1) Im Gegensatz zum Lupus-Biologikum Belimumab, das sich gegen das B-Zell-Zytokin BLyS oder BAFF richtet, bindet Ianalumab einen der Rezeptoren dieses Zytokins. Das verhindert einerseits natürlich die Aktivierung des Rezeptors. Andererseits ist Ianalumab aber ein depletierender Antikörper, der gleich auch noch die B-Zellen abräumt, die den BAFF-Rezeptor tragen. Ianalumab wird monatlich subkutan in einer Dosis von 300 mg verabreicht.
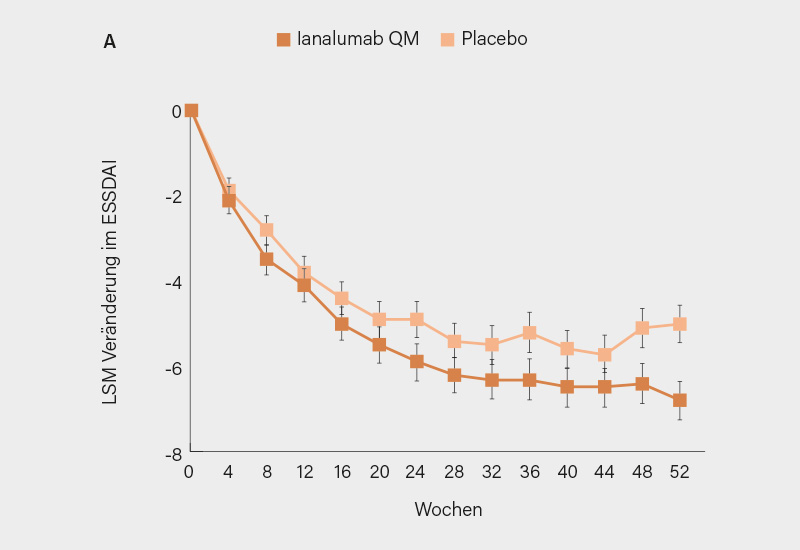
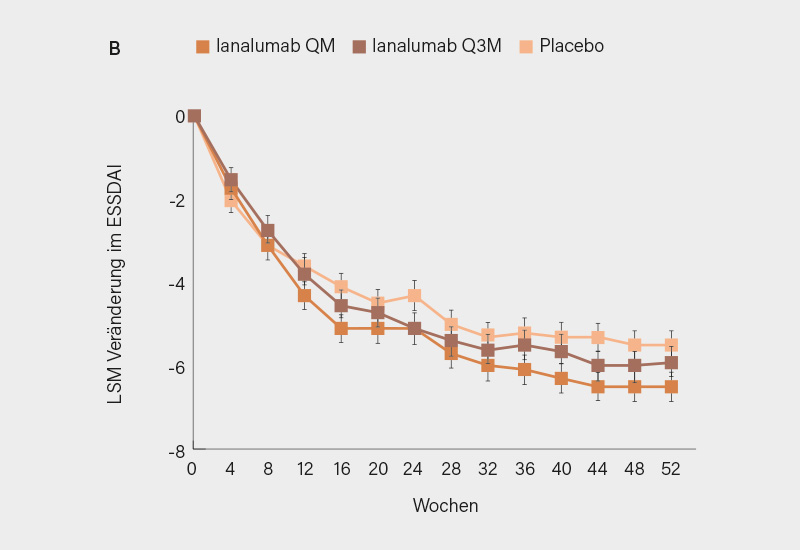
Die beiden doppelblinden, placebokontrollierten Studien erreichten trotz einer hohen Placebo-Antwort den primären Endpunkt, nämlich zu Woche 48 eine größere Verbesserung im EULAR Sjögren‘s Syndrome Disease Activity Index (ESSDAI) (Abb.), der im Wesentlichen Organmanifestationen und Immunologie der schweren SjD abbildet. Unterschiede zeigte aber auch die Globaleinschätzung der Krankheitsaktivität, nicht nur durch die Ärzte, sondern vor allem auch durch die Patientinnen und Patienten. Und bei denen, die noch einen nennenswerten Speicheldrüsenfluss >0,4 ml/min zu Baseline zeigten, stieg auch der Speichelfluss signifikant an. Zudem erwies sich Ianalumab als erstaunlich sicher; relevant scheinen vor allem Lokalreaktionen zu sein.
Noch nicht ganz so weit sind andere Ansätze, die alle im Wesentlichen im B-Zell- und Autoantikörper-Bereich angreifen. So wurde eine erfolgreiche chinesische Phase-III-Studie zu Telitacicept vorgestellt (2), das wie das aus Sicherheitsgründen nicht weiter verfolgte Atacicept als TACI-IgG-Konstrukt BLyS/BAFF und sein Schwester-Zytokin APRIL abfängt. Telitacicept war in allen Endpunkten sehr erfolgreich; es kam nicht zu relevanten Infektionen oder Hypogammaglobulinämien. Efgartigimod ist einer von mehreren Ansätzen, die sich gegen den neonatalen Fc-Rezeptor FcRn richten und über die Unterdrückung des IgG-Recycling Antikörper reduzieren. Hier wurde eine erfolgreiche Phase-II-Studie zur SjD vorgestellt. (3)
SYSTEMISCHER LUPUS ERYTHEMATODES
TLR-BLOCKADE ALT UND NEU
Hydroxychloroquin (HCQ) sollen nach den aktuellen EULAR-Empfehlungen alle SLE-Patientinnen und -Patienten in einer Dosis von 5 mg/kg Körpergewicht einnehmen, es sei denn, es gäbe klare Kontraindikationen. Diese Dosisempfehlung wurde durch einen systematischen Literaturüberblick bestätigt. (4) Oberhalb dieser Dosis vervierfacht sich fast das Retinopathie-Risiko (Hazard Ratio, HR 3,83), ist die Dosis geringer, steigt das Risiko von SLE-Schüben wiederum fast auf das Doppelte (HR 1,84). Auf Dauer dürfte sich aber die HCQ-Spiegelbestimmung als überlegen erweisen. Dort liegen nach einer Studie mit 1.842 Patientinnen und Patienten die Sollspiegel zwischen 750 und 1.150 ng/ml. (5) Darüber ist die Toxizität fast verdoppelt (HR 1,9), darunter die Schubrate um 40 % erhöht. Auch bei einer Solldosis von 5 mg/kg war die Hälfte im subtherapeutischen Bereich, während 18 % zu hoch dosiert waren – allerdings wurde die Dosis bei eingeschränkter Nierenfunktion nicht wie üblich halbiert, und eine chronische Niereninsuffizienz (CKD) im Stadium ≥3 war ein Risikofaktor.
Noch gezielter gegen die relevanten Toll-like-Rezeptoren (TLR) wirkende Substanzen sind mittlerweile in fortgeschrittener klinischer Prüfung. Aus der WILLOW-Studie zu Enpatoran, einem Antagonisten von TLR-7 und TLR-8, konnten Post-hoc-Daten eine fast drei Mal so hohe Remissionsrate von Lupus-Hauterscheinungen wie unter Placebo zeigen. (6)
TYP I-INTERFERON-REZEPTOR-BLOCKADE AUCH SUBKUTAN
Anifrolumab, das zweite zugelassene Biologikum bei SLE, musste bislang in Form einer monatlichen Infusionstherapie verabreicht werden. Dies ändert sich jetzt, nachdem Ende Dezember die europäische Zulassung für subkutanes Anifrolumab erteilt wurde. Als Poster vorgestellt wurde hierzu eine geplante Interimsanalyse der TULIP-SC-Studie (7), in der die Patientinnen und Patienten wöchentlich 120 mg Anifrolumab oder Placebo subkutan zusätzlich zur weiterlaufenden Standardtherapie erhielten. Das BILAG-based Composite Lupus Assessment (BICLA)-Ansprechen als primärer Endpunkt wurde nach 52 Wochen signifikant häufiger unter Anifrolumab (60 vs. 44 %) erreicht, in Kombination mit einer Prednisolon-Dosis von ≤7,5 mg täglich war der Unterschied noch etwas größer (59 vs. 40 %). Auch unter der subkutanen Gabe war die Differenzierung bereits ab Woche 12 eindeutig.
T2T: BAFF-REZEPTOR-, CD40-LIGANDEN- UND JAK-INHIBITION
Auch die Treat-to-target (T2T)-Ziele niedrige Krankheitsaktivität (Lupus Low Disease Activity State, LLDAS) und DORIS-Remission werden zunehmend als Endpunkte in SLE-Studien untersucht. Unter anderem waren Ianalumab (8), Dapirolizumab Pegol, das den CD40-Liganden bindet (9), und der Januskinase (JAK)-1-Inhibitor Upadacitinib (10) signifikant erfolgreicher als der Kontrollarm. Dapirolizumab brachte auch eine Verbesserung der Lupus-Fatigue mit sich. (11)
PROTEINURIE UND LUPUSNEPHRITIS
In den Empfehlungen der EULAR zum SLE und zur Lupus-Nierenbeteiligung wird ab einer neuen Proteinurie von 0,5 g/Tag oder 0,5 g/g Kreatinin im Spontanurin eine Nierenbiopsie empfohlen. Aus Baltimore kommende Daten zeigten zum Teil auch eine relevante Nephritis bei noch geringerer Eiweißausscheidung. (12) Dort wurden 28 Patientinnen und Patienten auch mit einer Protein-Kreatinin-Ratio von 0,2 bis 0,499 biopsiert, wenn sie nicht weiß waren, ein aktives Urinsediment, Komplementverbrauch oder Antikörper gegen doppelsträngige DNS (dsDNA) aufwiesen. 71 % hatten eine Lupusnephritis, allerdings kam keine Klasse IV und keine Klasse III + V vor. Sechs der 28 Biopsien zeigten eine Klasse III-Nephritis – nur in diesen Fällen war die Therapieindikation aus meiner Sicht eindeutig, und die Nephritis war dann immer assoziiert mit positiven Anti-dsDNA-Antikörpern und bei 5 von 6 mit Komplementerniedrigung. Das Urinsediment war in der Unterscheidung nicht hilfreich.
CERTOLIZUMAB PEGOL SCHÜTZT APS-SCHWANGERSCHAFT
Obwohl die Kombination aus niedermolekularem Heparin (NMH) und niedrig dosierter Acetylsalicylsäure (ASS) Aborte wegen Anti-Phospholipid-Antikörpern in vielen Fällen verhindern kann, bleibt insbesondere die Präeklampsie ein kaum beherrschbares Problem. Basierend auf Mausmodell-Daten, die eine direkte Rolle von TNF in dieser Pathologie zeigten, hat die IMPACT-Studie mit Certolizumab Pegol jetzt einen neuen Weg bei hohem Risiko aufgezeigt. (13) Insgesamt 57 Patientinnen mit Antiphospholipid-Syndrom (APS) und Frühschwangerschaft wurden eingeschlossen und von Woche 8 bis Woche 28 zusätzlich zur Antikoagulation mit Certolizumab Pegol behandelt.
Zu erwarten waren 40 % ungünstige Schwangerschaftsergebnisse, und 87 % der Patientinnen mit vorheriger Schwangerschaft hatten solch einen Endpunkt erlitten. Nur in zwei Fällen kam es zum Frühabort, vier weitere Aborte beruhten auf chromosomalen Aberrationen. Von den restlichen 51 Schwangerschaften endeten aber 48 mit einem lebend nach Hause entlassenen Baby.
CAR-T-ZELLEN UND BITE-ANTIKÖRPER: DIE HOFFNUNG AUF HEILUNG LEBT
Seit den 2021 publizierten ersten Erlanger Erfolgen steigt die Zahl der Beobachtungen zu CAR-T-Zellen bei Kollagenosen an – in Chicago waren es allein 14 Abstracts. Während nicht alle Konstrukte gleich erfolgreich sein dürften, bleibt es beim sensationellen Erfolg einer therapiefreien Remission bei zumindest einem Teil der SLE-Patientinnen und -Patienten und bei sehr positiven Ergebnissen auch bei anderen Kollagenosen. In Chicago wurden unter anderem Daten zu elf Patientinnen und Patienten mit Myositis gezeigt, die mit CAR-T-Zellen gegen CD19 behandelt wurden. (14) Darunter kam es zu einer dramatischen Besserung der Myositis, der Hautbeteiligung und der interstitiellen Lungenbeteiligung.
Während CD19 als Ziel beim SLE ziemlich eindeutig ist und bei den Autoimmun-Myositiden nach diesen Daten ausreicht, haben CAR-T-Zellen gegen CD19 bei der systemischen Sklerose (SSc) bislang nicht zu einem kompletten Verschwinden der spezifischen Autoantikörper geführt. Das gelang jetzt mit einem gegen das B-Zell-Reifungsantigen (BCMA) gerichteten Ansatz, wobei ein T Cell Engager, ein bispezifisch gegen CD3 und BCMA gerichteter (BiTE)-Antikörper verwendet wurde. (15) Ob die CAR-T-Zellen auf Dauer noch effektiver sind, wird sich erst mittelfristig herausstellen.
HÖHEPUNKTE JENSEITS DER KOLLAGENOSEN
SOMATISCHE MUTATIONEN ÜBER VEXAS HINAUS: IDH-1/2 IM FOKUS
Wenn ältere Patientinnen und Patienten autoinflammatorische Erkrankungen entwickeln, sind diese eher Folge somatischer Mutationen – also im Wesentlichen eines myelodysplastischen Syndroms – als von Keimbahnmutationen, wie wir seit der Entdeckung des VEXAS-Syndroms wissen. Die Isocitrat-Dehydrogenasen (IDH)-1 und -2 spielen im Citratzyklus eine Rolle und werden häufig in Malignomen gefunden. Von 265 bisher nicht diagnostizierten Patientinnen und Patienten mit systemischer Autoinflammation im Erwachsenenalter fanden sich bei 6 % solche Mutationen, nämlich acht im IDH-1- und sieben im IDH-2-Gen. (16) Der IDH-Inhibitor Ivosidenib führte bei ihnen zum Rückgang des CRP und der Neutrophilen-Zahlen. Zudem gab es in großen Kohorten Assoziationen der Mutationen in den IDH-Genen mit Riesenzellarteriitis (RZA) und Polymyalgia rheumatica.
RZA: SCHÜBE BEI ABSETZEN VON UPADACITINIB NACH EINEM JAHR
Upadacitinib ist nach dem Interleukin (IL)-6-Rezeptor-Blocker Tocilizumab die zweite für die RZA zugelassene Glukokortikoid (GK)-sparende Therapie. In Chicago wurden die 2-Jahres-Daten der SELECT-GCA-Studie vorgestellt. (17) Patientinnen und Patienten, die nach einem Jahr unter Upadacitinib in Remission waren, wurden für das zweite Jahr im Verhältnis 2:1 zur doppelblinden Weiterführung von Upadacitinib oder auf Placebo re-randomisiert. Unter weiterlaufender Upadacitinib 15 mg-Therapie blieben 69 % über das gesamte zweite Jahr in Remission, verglichen mit nur 29 %, die auf Placebo wechselten.
Auch wenn die Daten in der Realität mit vollem Monitoring der Entzündungsparameter etwas harmloser sein dürften, legen sie nahe, dass ein zweites Jahr Therapie in der Regel erforderlich sein wird. Erfreulicherweise gab es keine neuen Sicherheitssignale. Unter Upadacitinib (und weniger GK) kam es zu mehr Herpes Zoster, aber seltener zu schweren Infektionen. Es kam zu einer einzelnen venösen Thromboembolie unter Upadacitinib, und zu keinem einzigen schweren kardiovaskulären Ereignis oder gar Todesfall.
NEUES ZUR RA: ROSNILIMAB GEGEN ANTI-PD-L1-POSITIVE ZELLEN
Nachdem Abatacept als Hemmer der Kostimulation über CD80/86 und CD28 schon lange in der Therapie der rheumatoiden Arthritis (RA) verwendet wird, kommen jetzt auch Ansätze in Frage, die den zweiten Weg der Checkpoint-Inhibitoren über Programmed Cell Death (PD)-1 und seinen Liganden (PD-L1) beeinflussen. Rosnilimab bindet an T-Zellen, die viel PD-L1 an der Oberfläche tragen, und depletiert diese Zellen. In der nun vorgestellten Phase-IIb-Studie RENOIR (18) mit 424 RA-Patientinnen und -Patienten, von denen 41 % schon Biologika in der Vortherapie hatten, war Rosnilimab in allen drei Dosen (100 mg oder 400 mg vierwöchentlich oder 600 mg vierzehntägig) effektiv. Von den 319 Patientinnen und Patienten, die Rosnilimab erhielten, waren zu Woche 14 bereits 69 % in niedriger Krankheitsaktivität im CDAI, das ACR20-Ansprechen in Woche 12 lag in der höchsten Dosis bei über 75 %. Nachdem die Substanz in Woche 28 gestoppt wurde, hielt die Wirksamkeit bei drei Viertel noch weitere drei Monate an. Es wurden keine Todesfälle, Malignome oder schweren Infektionen beobachtet.
Im Gegensatz dazu traten unter dem PD-1-aktivierenden Antikörper Peresolimab in den höheren beiden Dosen vier Malignome auf – und keines in den beiden anderen Armen. (19) Bei zudem deutlich weniger beeindruckenden Effektivitätsdaten wurde die Entwicklung daher eingestellt.
TYK-2-INHIBITOR NUN AUCH FÜR PSORIASIS-ARTHRITIS
Die Tyrosinkinase-2 (TYK-2), das vierte Mitglied der Januskinase-Familie, ist für die Signaltransduktion von Typ-I-Interferonen und von IL-12 und IL-23 wichtig. Der TYK-2-Inhibitor Deucravacitinib ist bereits für die Psoriasis zugelassen. Die POETYK-PsA-1-Studie zeigte jetzt auch die Wirksamkeit für die Psoriasis-Arthritis (PsA) über bis zu 52 Wochen. (20) In Woche 16 erreichten 54 % der 336 Patientinnen und Patienten unter Deucravacitinib, aber nur 34 % der 334 im Placebo-Arm die ACR20-Antwort. Auch die anderen PsA-Domänen verbesserten sich deutlicher als unter Placebo. Das Sicherheitsprofil war günstig, mit nur etwa 6 % schweren unerwünschten Ereignissen und dem Ausbleiben von Todesfällen, jedoch traten bei manchen Patienten Akne oder andere Hautausschläge auf.
ASAS-SPARTAN-KLASSIFIKATION FÜR AXIALE SPONDYLOARTHRITIS
Mit dem ehrgeizigen Ziel einer Spezifität von ≥90 % und einer Sensitivität von ≥75 % wurden reale Daten von 1.015 Patientinnen und Patienten mit mindestens 3 Monaten Rückenschmerz und Auftreten vor dem 45. Lebensjahr analysiert, von denen 370 (36,4 %) eine axiale Spondylarthritis (axSpA) hatten. Das Ergebnis dieser Kollaboration von ASAS und SPARTAN ist ein gewichteter Score mit einem Cut-off von 11 Punkten, wobei das positive MRT 8 Punkte, positive Röntgenaufnahmen 7 Punkte, positives HLA-B27 4 Punkte und inflammatorischer Rückenschmerz 3 Punkte zählen – und alles andere, von erhöhtem CRP über periphere Arthritis und Fersenenthesitis bis zu Psoriasis, chronisch-entzündlicher Darmerkrankung (CED) und anteriorer Uveitis, je 1 Punkt. (21)
NEUROTROPHIN-INHIBITION ALS MÖGLICHER ANSATZ FÜR DIE ARTHROSE-THERAPIE
Abschließend noch ein Studienergebnis, das Hoffnung auf eine vielleicht doch mögliche medikamentöse Arthrose-Therapie aufkommen lässt. LEVI-04 ist ein Fusionsprotein aus IgG (Fc-Teil) und dem p75 Neurotrophin-Rezeptor, das Neutrotrophin-3 inhibiert. Insgesamt 518 Patientinnen und Patienten mit symptomatischer Gonarthrose wurden auf Placebo oder einen von drei LEVI-04-Dosisarmen (0,3, 1 oder 2 mg/kg) randomisiert. (22) Das Fusionsprotein zeigte im MRT eine dosisabhängige Abnahme des Knochenmarksödems, insbesondere in fortgeschrittenen Krankheitsstadien (Kellgren-Lawrence Grad 3 und 4).
Selbst für die in den letzten Jahrzehnten von Erfolgsgeschichten geradezu verwöhnte Rheumatologie zeigte der Kongress in Chicago wieder beeindruckende Fortschritte auf ganz verschiedenen Gebieten. Manche der erwähnten Therapien werden vermutlich bald auch in Deutschland in diesen Indikationen zur Verfügung stehen, und auch für die Patientinnen und Patienten mit heute noch schlecht behandelbaren Erkrankungen gibt es Hoffnung auf neue Ansätze.
Prof. Dr. med. univ. Martin Aringer
Bereichsleiter Rheumatologie
Medizinische Klinik und Poliklinik III
Universitätsklinikum Carl Gustav Carus
an der Technischen Universität Dresden
Fetscherstraße 74, 01307 Dresden
Quellen: 1 Grader-Beck T et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB24 | 2 Xu D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB11 | 3 Peene I et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0694 | 4 Nestor J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0805 |5 Garg S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1722 | 6 Morand E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0802 | 7 Manzi S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 1545 | 8 Morand E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0801 | 9 Morand E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0645 | 10 Morand E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2445 | 11 Morand E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0644 | 12 Petri M et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0772 | 13 Salmon J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0855 | 14 Aggarwal R et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB14 | 15 Györfi A-H et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0678 | 16 Castellan F et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB21 | 17 Schmidt W et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0776 | 18 Graf J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB19 | 19 Tuttle J et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0473 | 20 van der Heijde D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB20 | 21 Maksymowych W et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0854 | 22 Westbrook S et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0852