Im Hinblick auf potenzielle neue Therapien mit Abstand am spannendsten war eine von Frank Buttgereit, Berlin, präsentierte 24-wöchige, internationale, randomisierte, doppelblinde, Doppel-Dummy, aktiv-kontrollierte Phase-IIa Proof-of-Concept-Studie zur Effektivität und Sicherheit eines Konjugats aus Adalimumab und einem hoch potenten GRM bei Patienten mit mäßiger bis schwerer aktiver RA. Verglichen wurde hierin i.v. ABBV-3373 100 mg (für 12 Wochen gefolgt von Placebo für 12 Wochen) mit s.c. Adalimumab 80 mg alle 2 Wochen für 24 Wochen bei Patienten auf Methotrexat (MTX). Primärer Endpunkt war die Verbesserung im DAS28-CRP von Baseline bis Woche 12. Ein weiterer präspezifizierter Vergleich erfolgte gegen historische Adalimumab-Daten alleine und kombiniert mit den In-Trial-Daten. Überdies wurde ein Propensity Score-gematchter Placeboarm (n=96) mit einbezogen. Sekundäre Endpunkte in Woche 12 waren der ΔCDAI, ΔSDAI, ΔDAS28-ESR, ΔHAQ-DI sowie Anteil von Patienten mit einem DAS28-CRP ≤3,2, das ACR20/50/70-Ansprechen und ein minimal klinisch bedeutsamer Rückgang im HAQ-DI ≤-0,22. Therapieassoziierte unerwünschte Ereignisse (TEAE) wurden in Woche 12 erfasst.
Positive Phase-II-Daten für neuartiges Anti-TNF/GRM-Konjugat
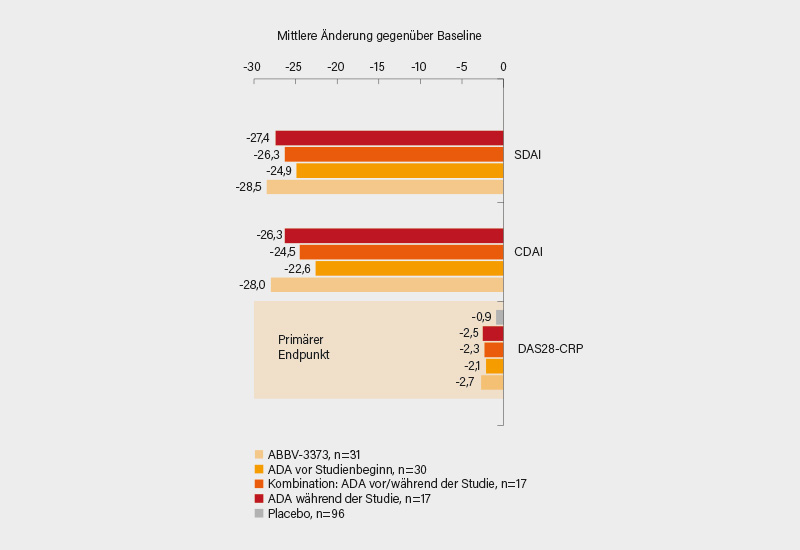
Im Verhältnis 2:1 wurden 48 Patienten mit etablierter RA auf ABBV-3373 (n=31) oder Adalimumab (n=17) randomisiert, 96 % schlossen die 12-wöchige Behandlungsphase ab. Im Ergebnis bot bei vergleichbarer Ausgangssituation (Demografie, Krankheitscharakteristika) ABBV-3373 eine signifikante Verbesserung im durchschnittlichen DAS28-CRP in Woche 12 gegenüber der prä-spezifizierten historischen Adalimumab-Kohorte (-2,65 vs. -2,13; p=0,022) und schnitt numerisch besser als der kombinierte In-trial und historische Adalimumab-Arm ab (-2,65 vs -2,29) (Abb.). Vergleichbare Verbesserungen der Krankheitsaktivität wurden unter ABBV-3373 und der In-trial Adalimumab-Kohorte gesehen. Diese beiden Therapiearme waren der synthetischen Placebogruppe signifikant überlegen (p<0,001). Für die sekundären Endpunkte zeigte sich eine größere Effektivität von ABBV-3373 gegenüber der historischen Adalimumab-Kohorte und mit einer prädizierten Wahrscheinlichkeit von 79-99 % auch im Vergleich zur kombinierten In-trial und historischen Adalimumab-Kohorte. Die Verträglichkeit von ABBV-373 gegenüber In-trial Adalimumab war gut (UE: 35,5 vs. 70,6 %; TEAE 6,5 vs. 17,6 %). Es gab 2 schwere Infektionen unter ABBV-3373 und keine unter Adalimumab. Auch kam es zu einem anaphylaktischen Schock unter ABBV-3373, woraufhin die Dauer der i.v.-Applikation von 3 auf 15-30 min. gesteigert wurde. Bei einem ähnlichen Sicherheitsprofil bieten diese ersten Daten Anlass zur Hoffnung auf eine potenziell bessere Effektivität des neuen Konjugats, die es jetzt in größeren Studien zu evaluieren gilt. (1)
bDMARDS und JAKi: Bei Älteren nicht mehr schwere Infektionen
Bei älteren Patienten (>70 Jahre) werden bDMARDs und JAKi aufgrund von Komorbiditäten oder des hohen Alters als bekannten Risikofaktoren für schwere Infektionen (SIE) oft eher zögerlich eingesetzt. Anja Strangfeld, Berlin, präsentierte nun eine Analyse des RABBIT-Registers, in dem das Risiko für solche Ereignisse unter bDMARDs und JAKi speziell in dieser Altersgruppe untersucht wurde.
Eingeschlossen wurden 2.274 ältere RA-Patienten, von denen 425 insgesamt 616 SIE entwickelten. Ältere Patienten auf bDMARDs hatte eine längere Krankheitsdauer und höhere Krankheitsaktivität als solche auf csDMARDs. 62-73 % der Patienten hatten mehr als drei Komorbiditäten. Während erwartungsgemäß bei Älteren mehr SIE (6,6/100 Patientenjahre) als bei Patienten <70 Jahre auftraten, gab es im älteren Kollektiv keine signifikanten Unterschiede zwischen mit csDMARDs, TNFi, Rituximab, IL-6i, Abatacept oder JAKi behandelten Patienten (Hazard ratios, HR ~0,9). Faktoren, die SIE in die Höhe trieben waren primär Komorbiditäten (vor allem COPD und Lungenfibrose mit einer HR von 1,8 sowie Niereninsuffizienz und Typ-2-Diabetes) und eine höhere Krankheitsaktivtät (HR 1,1) sowie sekundär und eher untergeordnet Glukokortikoide (GK). (2)
Schwangerschaft: Risiko vor allem von Krankheitsaktivität getrieben
Über das Outcome von Schwangerschaften von RA-Patientinnen berichtete Karin Hellgren, Stockholm (Schweden). Bekanntlich tragen diese ein höheres Risiko insbesondere im Hinblick auf Früh- und Mangelgeburten (SGA = small for gestational age). Anhand von schwedischen und dänischen Rheuma- und nationalen Geburtenregistern wurden 1.739 RA-Schwangerschaften identifiziert und einer Kohorte von 17.390 Kontroll-Schwangerschaften gegenübergestellt.
Wie erwartet waren RA-Schwangerschaften mit einem höheren Risiko von Frühgeburten (Odds ratio, OR 1,92) und SGA-Geburten (OR 1,93) assoziiert. Bei RA-Patientinnen mit bekanntem DAS28-CRP erhöhten Werte ≥3,2 versus <3,2 das Risiko für Früh- und SGA-Geburten (OR 2,69 bzw. 3,39). Die Stratifizierung nach verschiedenen medikamentösen Therapien änderte kaum etwas an diesen Befunden – die Höhe der Krankheitsaktivität in der Schwangerschaft scheint maßgeblich das Risiko zu bestimmen, sodass gerade bei intensiv behandelten RA-Patientinnen mit residualer Aktivität ein sorgfältiges Monitoring während der Schwangerschaft erforderlich ist. (3)
Update zu den Therapieoptionen bei RA-assoziierter ILD
Auf Basis der INBUILD-Studie wurde der Multi-Tyrosinkinase-Inhibitor Nintedanib auch bei progredient-fibrosierenden ILDs jenseits der idiopathischen Lungenfibrose (IPF) und der systemischen Sklerose (SSc) zugelassen. Im Gesamtkollektiv der Phase-III-Studie hatte Nintedanib die jährliche Abnahme der forcierten Vitalkapazität (FVC; ml/Jahr) um 57 % reduziert. Eingeschlossen waren die Kriterien einer progressiven ILD erfüllende Patienten mit einer Fibrose ≥10 % in der HRCT, Vitalkapazität (FVC) ≥45 % und Diffusionskapazität (DLCO) zwischen ≥30 und <80 %. Von den insgesamt 663 Teilnehmern hatten 89 eine RA-ILD (davon erhielten 42 Nintedanib), deren Ergebnisse von Clive Kellly, Newcastle (Großbritannien), vorgestellt wurden. Am häufigsten war mit 86,5 % ein UIP-Muster in der HRCT. 21 % erhielten zu Baseline überdies ein bDMARD, 54 % csDMARDs und 73 % GK.
Nach 52 Wochen war der FVC-Verlust unter Nintedanib versus Placebo signifikant geringer (-82,6 vs. -199,3 ml/Jahr; nominal p=0,037), was recht gut den Befunden im Gesamtkollektiv entsprach. Die Nebenwirkungen, vor allem Diarrhöen, waren meistens beherrschbar, die Abbruchrate unter Nintedanib war aber etwas höher (19 vs. 12 %). (4)
Auch die ohnehin bei RA eingesetzten Therapien haben vielfach positive Effekte auf die ILD, so etwa Rituximab, Tocilizumab oder Abatacept. Zu letzterem wurde von Belen Atienza-Mateo, Santander (Spanien), eine neue Analyse einer multizentrischen Studie mit 190 RA-ILD-Patienten präsentiert. Dass Abatacept wirksam war überraschte nicht, wohl aber, dass die Effektivität im Hinblick auf eine Stabilisierung von FVC und DLCO bei Patienten mit UIP- und NSIP-Muster in der HRCT vergleichbar gut war. Ein früher Einsatz noch vor Ausbildung größerer Schäden durch die ILD scheint vorteilhaft zu sein. (5)
Kurz erwähnt seien noch Real-life-Daten des TReasure-Registers zu 47 mit Tofacitinib behandelten RA-ILD-Patienten, die Umut Kalyoncu, Ankara (Türkei), präsentierte. Hierin fanden sich Hinweise auf einen versus Baseline guten Erhalt der Lungenfunktion unter Tofacitinib nach median 12 Monaten (Einsekundenkapazität, FEV1: 82,1 vs. 82,8 %;, FVC: 79,8 vs. 82,8 %), erkauft jedoch mit vielen infektionsbedingten Abbrüchen der JAKi-Therapie. (6)
Quellen:
1 Ann Rheum Dis 2021; 80(Suppl1): 64 (OP0115)
2 Ann Rheum Dis 2021; 80(Suppl1): 64-65 (OP0116)
3 Ann Rheum Dis 2021; 80(Suppl1): 126 (OP0210)
4 Ann Rheum Dis 2021; 80(Suppl1): 69 (OP0124)
5 Ann Rheum Dis 2021; 80(Suppl1): 531-532 (POS0595)
6 Ann Rheum Dis 2021; 80(Suppl1): 69-70 (OP0125)