Über 50 % der RA-Patienten benötigen mehrere unterschiedliche b/tsDMARDs aufgrund unzureichenden Ansprechens oder Wirkverlust. Rosnilimab ist ein monoklonaler Antikörper, der gezielt pathogene T-Zellen (insbesondere PD-1hoch, Tph/Tfh, Teff) angreift und eliminiert. In die von Jonathan Graf, San Francisco (USA), und internationalen Kollegen als Late breaking-Abstract präsentierte randomisierte, doppelblinde, placebokontrollierte Phase-IIb-Studie RENOIR wurden 424 erwachsene Patienten mit moderater bis schwerer (SJC und TJC je ≥6) seropositiver RA (95,0 % und 86,6 % waren RF- bzw. ACPA-positiv) ein, die gleichzeitig csDMARDs und <3 vorherige b/tsDMARDs (41 % waren mit b/tsDMARDs vorbehandelt) erhielten. Die Teilnehmer (mittlerer DAS28-CRP 5,6, CDAI 37,7, CRP-Wert 18 mg/l) wurden im Verhältnis 1:1:1:1 auf s.c. Rosnilimab 100 mg alle 4 Wochen (Q4W), 400 mg Q4W, 600 mg Q2W oder Placebo randomisiert. Primärer Endpunkt war die mittlere Veränderung des DAS28-CRP gegenüber dem Ausgangswert in Woche 12. Teilnehmer, die Rosnilimab erhielten, mussten in Woche 14 eine niedrige Krankheitsaktivität (LDA) gemäß CDAI ≤10 erreichen, um sich für die verblindete zweite aktive Therapiephase (nur Rosnilimab) bis Woche 28 zu qualifizieren, gefolgt von einem Off-Drug-Follow-up bis Woche 38.
Überzeugende Phase-II-Daten zu Rosnilimab
Der primäre Endpunkt, die Reduktion des DAS28-CRP gegenüber dem Ausgangswert in Woche 12, wurde mit allen Rosnilimab-Dosen erreicht (-2,06, -2,12, -2,06 in der 100 mg-, 400 mg- und 600 mg-Gruppe) gegenüber Placebo (-1,69) (p<0,01). Zu Woche 12 zeigte sich für alle Rosnilimab-Dosierungen ein versus Placebo signifikant größeres ACR20-Ansprechen (68,9, 70,1 und 75,2 % vs. 52,8 %) und eine größere Abnahme des (hs)CRP-Werts (-9,67, -10,10 und -7,60 vs. -0,73). Auch im ACR50- (44,3, 36,4 und 46,7 % vs. 33,0 %) und ACR70-Ansprechen (21,7, 21,5 und 21,9 % vs. 17,9 %), dem Erreichen einer CDAI LDA (46,2, 49,5 und 38,1 % vs. 31,1 %) sowie in Patient Reported Outcomes (PROs) wie Patientenurteil (PGA), HAQ-DI und Schmerz (VAS) zeigte sich ein konsistent besseres Ansprechen des neuen Wirkprinzips. Insgesamt 69 % der mit Rosnilimab behandelten Patienten erreichten eine CDAI LDA zu Woche 14 und gingen in die zweite Therapiephase ein, jene, die dieses Ziel verfehlten, wurden bei künftigen Visiten als Non-Responder imputiert (obwohl auch von diesen 60 bzw. 18 % ein ACR20/50-Ansprechen erzielt hatten).
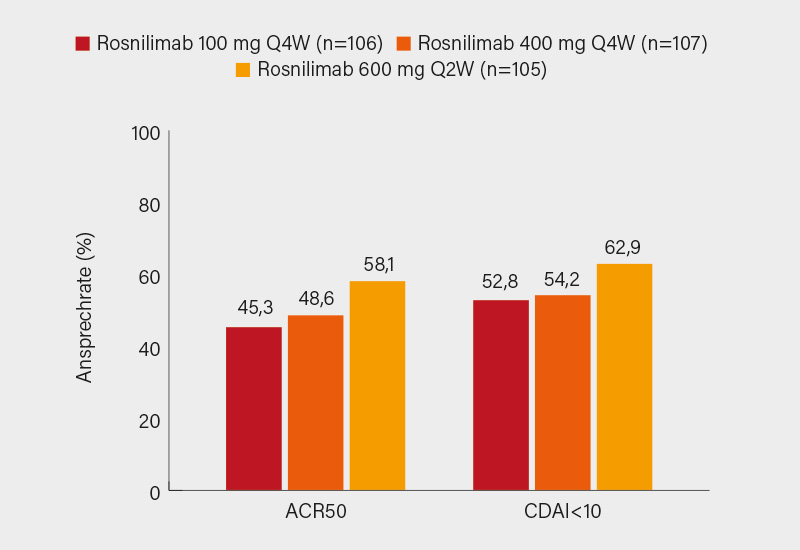
Von Woche 12 bis 28 kam es unter Rosnilimab 100 mg Q4W, 400 mg Q4W und 600 mg Q2W zu einem weiteren Anstieg des Ansprechens in den sekundären Endpunkten, so im ACR50 auf 45,3, 48,6 und 58,1 % (Abb.), im ACR70 auf 40,6, 36,4 und 44,8 % sowie bei der CDAI LDA ≤10 auf 52,8, 54,2 und 62,9 % (Abb.). Dasselbe Bild zeigte sich in Woche 28 für DAS28-CRP (bis zu -2,56), PGA (bis zu -40,1), HAQ-DI (bis zu -0,75) und Schmerz VAS (bis zu -46,7). Nach Woche 26 blieb während des 12-14-wöchigen Off-Drug-Follow-up das Ansprechen im Wesentlichen erhalten – so behielten 78-84 % der Teilnehmer das zu Woche 28 erreichte ACR50-Ansprechen bis Woche 38, 67-77 % das ACR70-Ansprechen und 75-82 % die CDAI LDA. Die Ergebnisse waren bei b/tsDMARD-naiven und -erfahrenen Patienten vergleichbar. Translationale Daten zeigten eine rasche Depletion (>90 %) pathogener T-Zellen im Blut bei gleichzeitiger Erhaltung der Gesamtzahl der T-Zellen über 28 Wochen. Auch Synovialbiopsien in Woche 6 belegen eine >90 %ige Depletion pathogener T-Zellen sowie eine breite Herunterregulierung von Genexpressionsmustern einschließlich der Aktivierung von T-, B- und Myeloidzellen. Rosnilimab wurde insgesamt gut vertragen. 7 % der Teilnehmer brachen die Studie vor Woche 12 ab, 4 % in der zweiten Therapiephase. Es wurden keine Todesfälle oder Malignome gemeldet, auch traten keine schweren Infektionen auf, die zum Studienabbruch führten. Rosnilimab bot somit klinisch relevante, andauernd hohe Ansprechraten. (1) Auf Phase-III-Studien ist zu hoffen, angekündigt sind solche aber noch nicht.
Weitere Neuigkeiten aus Chicago im Überblick
Weniger gut lief eine von Michael Weinblatt, Boston (USA), und internationalen Kollegen vorgestellte Phase-IIb-Studie zu dem den Immuncheckpoint-Rezeptor PD-1 stimulierenden monoklonalen IgG1-Antikörper Peresolimab, der zuvor in Phase-IIa erfolgreich bei RA-Patienten mit unzureichendem DMARD-Ansprechen erprobt wurde. In der neuen Studie blieb das Ansprechen nach 12 Wochen klar unter den Erwartungen (ein ACR20-Ansprechen wurde von max. 52 % der 490 Patienten erreicht), zugleich wurden mehrere Malignitäten und MACE (bis Woche 60) berichtet (2), sodass die weitere Entwicklung gestoppt wurde.
Ein neuer, von US-amerikanischen Experten um Minna Kohler, Boston, in einer Phase-I-Pilotstudie verfolgter Ansatz besteht in der Anwendung autologer CAR-Treg (regulatorische T-Zellen)-Zellen bei therapierefraktären RA-Patienten (Versagen auf ≥3 b/tsDMARD-Klassen) mit einem DAS28-CRP ≥3,2. Das CAR war spezifisch für citrullinierte Proteine (CitP), anders als bei klassischen CAR-T-Zelltherapien ist keine vorherige Lymphodepletion erforderlich. Bislang wurden 6 Patienten CitP-spezifische CAR-Treg-Zellen in unterschiedlich hohen Dosierungen infundiert (eine einzelne i.v.-Gabe) und bei je zwei Dritteln eine Reduktion des SJC/TJC um ≥50 % und des DAS28-CRP um ≥2 erreicht, schwere Nebenwirkungen wie ein CRS oder Neurotoxizität wurden nicht verzeichnet. Weitere Daten bleiben abzuwarten. (3) Von Fredrik Albach, Berlin, und Kollegen gezeigte frühe Daten der deutschen COMPARE-Studie zum Einsatz einer „klassischeren“ CD19 CAR-T-Zelltherapie mit CD28-Kostimulation (KYV-101) bei 6 therapierefraktären RA-Patienten zeigen auch, dass dieses Verfahren nicht immer funktioniert. Trotz klarer Effekte wie B-Zell-Depletion sowie Rückgang von ACPA und RF erreichten bislang nur zwei Drittel ein ACR20- und ein Drittel ein ACR50-Ansprechen. (4)
Abschließend noch zu den bereits verfügbaren Therapien. In Chicago noch nicht präsentiert, aber bereits vorab gemeldet wurden Top Line-Resultate der Phase-IIIb/IV-Studie SELECT-SWITCH mit (nach TNF-Inhibitor-Versagen/-Intoleranz) dem Head-to-head (H2H)-Vergleich eines Cyclings mit Adalimumab (40 mg Q2W) oder Switchens auf Upadacitinib (15 mg/Tag): In Woche 12 erreichten mehr Patienten unter Upadacitinib den primären Endpunkt (DAS28-CRP ≤3,2: 43,3 vs. 22,4 %) und wichtigsten sekundären Endpunkt (DAS28-CRP <2,6: 28,4 vs. 14,5 %). In Bezug auf Methotrexat (MTX) zeigte eine kleine randomisiert-kontrollierte Studie französischer Rheumatologen um Claire Immediato Daien, Montpellier, dass eine Ballaststoff-Supplementation (Inulin, 12 g/Tag) das Ansprechen auf MTX steigern kann. Bei den 49, im Verhältnis 1:1 randomisierten RA-Patienten erhöhte sich unter MTX plus Inulin signifikant die Wahrscheinlichkeit eines EULAR-Ansprechens (Odds Ratio, OR 4,65; p=0,03) und reduzierte zirkulierende Th17-Zellen sowie das Th17/Treg-Verhältnis (p=0,02). Die DAS28-Reduktion der MTX-Anwender betrug -1,00 mit Inulin vs. -0,34 unter Placebo. Sollten sich diese Daten bestätigen, könnte dies Konsequenten für die tägliche Praxis haben. (5) Nur kurz erwähnt sei die inzwischen publizierte randomisierte, placebokontrollierte Phase-II-Studie StopRA von Kevin Deane, Aurora (USA), und Kollegen. Bei Risikopatienten für die Entwicklung einer RA (stark erhöhter anti-CCP3-Spiegel) führte eine präventive Gabe von Hydroxychloroquin (HCQ) über 12 Monate nicht zu einer Reduktion des Risikos für eine klinisch manifeste RA oder entzündliche Arthritis nach 36 Monaten. (6)
Wenn es schon schwierig ist, eine RA zu verhindern, wäre es zumindest möglich, eine difficult-to-treat (D2T)-RA zu vermeiden? Eine belgische 25-Jahres-Studie lässt darauf schließen, dass fast 25 % der Patienten eine D2T-RA entwickeln – dies seltener, wenn frühzeitig bDMARDs eingesetzt werden. (7) Britische Experten um Task Toyoda, fanden wiederum nach fünf Jahren, dass es bei initial mit TNF-Inhibitoren versus csDMARDs behandelten Patienten seltener zu einer D2T-RA kommt (1 vs. 7 %). Nach zehn Jahren wurde zudem häufiger eine anhaltende Remission verzeichnet (62 vs. 45 %; p=0,014). (8)
Quellen:
1 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. LB19
2 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. 0473
3 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. LB23
4 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. 0471
5 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. LB15
6 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. 1674
7 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. 1679
8 Arthritis Rheumatol 2025; 77(Suppl. 9): Abstr. 1677