Die vornehmlich rheumatologisch geprägte Expertengruppe um Erstautor Prof. Henes und Prof. Dr. Norbert Blank, Heidelberg, der als Leitlinienkoordinator fungierte, konsentierte insgesamt acht übergeordnete sowie 63 spezifische Empfehlungen.
Übergeordnete Empfehlungen
Eine zentrale Botschaft ist, dass SSc-Erkrankte interdisziplinär versorgt und an einem Zentrum für SSc behandelt werden sollen. Eine frühe Diagnosestellung und eine rasche Therapieeinleitung sind wichtig, um Organschäden zu vermeiden, Schmerzen zu reduzieren und die Beweglichkeit zu erhalten. Wichtig ist ebenfalls, dass Patientenschulung und partizipative Entscheidungsfindung Teil der Behandlung sein sollen. Die Aktivität und Ausprägung der SSc sollen durch regelmäßige Untersuchungen, unter Zuhilfenahme der jeweiligen (validierten) Instrumente und diagnostischen Methoden überwacht werden. Die medikamentöse Behandlung soll sich nach dem individuellen Risikoprofil der Erkrankten, Komorbiditäten und der am schwersten betroffenen Organmanifestation orientieren. Patienten-adaptierte physikalische Therapiemodalitäten sowie Kälteschutz, Schutz vor Verletzungen, Nikotinkarenz, Verzicht später Mahlzeiten bei ausgewogener Ernährung und regelmäßige sportliche Betätigung sowie rehabilitative Maßnahmen sollen Teil einer jeden SSc-Behandlung sein. Last but not least sollte bei jedem SSc-Erkrankten eine Teilnahme im DNSS-Register und an einer Therapiestudie geprüft werden.
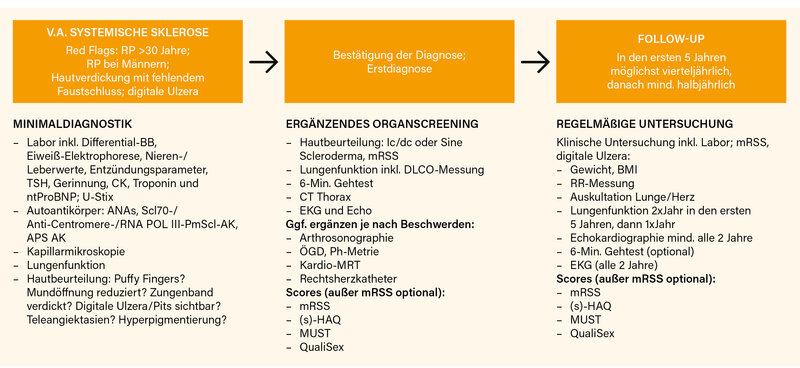
Den spezifischen Empfehlungen zu einzelnen Manifestationen bzw. Organbeteiligungen vorangestellt werden allgemeine Empfehlungen zur körperlichen Untersuchung, Labor und Scores bzw. Fragebögen (Abb. 1).
Hautsklerose
Die Hautsklerose sollte mit Hilfe des modifizierten Rodnan Skin-Scores (mRSS) beurteilt werden. Eine progrediente Hautsklerose soll immunsuppressiv behandelt werden – die Evidenz für spezifische Substanzen ist hier generell gering. Bei Hautsklerose und bei funktionellen Einschränkungen sollen frühzeitig Lymphdrainagen und Physiotherapie eingesetzt werden. Systemische Glukokortikoide (GK) sollten nicht für die Therapie der Hautsklerose eingesetzt werden. Eine etablierte Therapie der Calcinosis cutis ist nicht belegt.
Periphere vaskuläre Störungen
Bei Abklärung eines Raynaud-Phänomens (RP) soll die SSc als prognostisch bedeutsame Differentialdiagnose stets erwogen werden. Regelmäßige Evaluationen sollen bezüglich RP, trophischen Veränderungen und digitalen Ulzera (DU) erfolgen. Zur RP-Abklärung sollen Kapillarmikroskopie und Auto-Antikörper-Diagnostik eingesetzt werden. Bei V. a. Digitalarterienverschlüsse sollte das Vorliegen einer Makroangiopathie abgeklärt werden. Bei RP kann der Einsatz von Calciumkanalblockern (CKB) vom Dihydropyridintyp erwogen werden. Beim schwerem RP oder DU sollen Phosphodiesterase (PDE)-5-Inhibitoren oder i.v. Prostazyklinanaloga (präferentiell Iloprost) zum Einsatz kommen. Bei refraktärem RP können AT-I-Rezeptorblocker (ARB), selektive Serotonin-Reuptake–Hemmer (SSRI) oder eine topische Behandlung mit nitrathaltigen Salben erwogen werden. Bei DU soll der Endothelinrezeptor-Antagonist (ERA) Bosentan zur Anwendung kommen, um neuen Ulzera vorzubeugen. Bei V. a. Digitalarterienverschlüsse kann der Einsatz von Thrombozytenaggregationshemmer (ASS 100 mg/Tag) erwogen werden. Bei Makroangiopathie und arteriosklerotischen Veränderungen soll eine medikamentöse Sekundärprophylaxe nach aktuell gültigen Leitlinien erfolgen.
Lungenbeteiligung/ILD
Bei Erstdiagnose einer SSc sollen Auskultation, Lungenfunktion (mit DLCO-Bestimmung) und eine Dünnschicht-CT Thorax-Untersuchung erfolgen. Bei allen SSc-Erkrankten sollen regelmäßige Auskultationen der Lunge und Lungenfunktions-Tests erfolgen. Bei neuen Auffälligkeiten soll eine Dünnschicht-CT Thorax ergänzt werden. Bei Erkrankten mit nachgewiesener Progression der SSc-assoziierten interstitiellen Lungenerkrankung (ILD) oder Risikofaktoren soll eine immunsuppressive Therapie durchgeführt werden (als First-line-Therapien werden hier Mycophenolat Mofetil [MMF] und Cyclophosphamid [CYC], genannt). Bei SSc-ILD sollte eine antifibrotische Therapie durchgeführt werden (im Regelfall Nintedanib). Bei SSc-ILD und einer Refluxkrankheit (GERD) sollen PPIs eingenommen werden.
Pulmonale (arterielle) Hypertonie
Diagnostik und Therapie der pulmonalen Hypertonie bei SSc sollen gemäß den Leitlinien kardiologischer und pneumologischer Fachgesellschaften erfolgen. Bei SSc soll eine jährliche Risikobeurteilung bezüglich einer pulmonalen Hypertonie durchgeführt werden. Neben Anamnese und körperlicher Untersuchung sollten Biomarker (z. B. NT-proBNP) bestimmt und eine Echokardiographie erwogen werden. Ausgehend von den Befunden des Screenings soll die Indikation für eine Rechtsherzkatheter-Untersuchung überprüft werden (z. B. nach DETECT-Algorithmus). Auch bei ungeklärter persistierender Dyspnoe soll ein Rechtsherzkatheter durchgeführt werden. Die initiale Therapie einer pulmonal arteriellen Hypertonie soll bei fehlenden Kontraindikationen mit einer Kombination aus ERA und PDE-5-Inhibitor erfolgen.
Kardiale Beteiligung
Eine Herzbeteiligung soll initial durch Anamnese, körperliche Untersuchung, Biomarker (Troponin, BNP/NT-proBNP), EKG, Langzeit-EKG und Echokardiographie evaluiert werden. Bei Hinweisen auf eine Herzbeteiligung sollte ein Kardio-MRT durchgeführt werden. Verlaufskontrollen sollten nach individueller Abwägung erfolgen. Eine Myokardbiopsie zur Abklärung einer primären SSc-Herzbeteiligung soll nicht routinemäßig durchgeführt werden. Bei V. a. eine primäre SSc-Herzbeteiligung sollte das akute Koronarsyndrom als Differentialdiagnose erwogen werden und gemäß der aktuellen kardiologischen Leitlinie abgeklärt werden. Eine Pharmakotherapie mit Antiarrhythmika, der Herzinsuffizienz bzw. KHK, Schrittmacher- bzw. Kardioverter-Defibrillator-Therapie und elektrophysiologische Ablationen sollten gemäß den kardiologischen Leitlinien erfolgen. Bei Erkrankten mit primärer SSc-Herzbeteiligung sollte eine immunsuppressive Therapie durchgeführt werden. Zur Verlaufskontrolle bei SSc-Herzbeteiligung sollten mindestens alle 6 Monate BNP/NT-proBNP und Troponin bestimmt, und mindestens einmal jährlich eine Echokardiographie sowie ein Ruhe-EKG und Langzeit-EKG durchgeführt werden.
Zahn-, Mund- und/oder Kieferbeteiligung
Bei SSc-Erkrankten sollte initial und mindestens einmal jährlich eine genaue Erhebung von Zahn- und Parodontalstatus und die Inspektion aller Mundschleimhautregionen erfolgen, insbesondere bei eingeschränkter Mundöffnung. Zur Erfassung einer Verbreiterung des Parodontalspaltes (Frühsymptom) und Knochenresorptionsprozessen (Spätsymptom) sollte eine radiologische Diagnostik durchgeführt werden. In Abhängigkeit vom Schweregrad der Mitbeteiligung des Kauorganes und einer eingeschränkten Hand- und Fingermobilität bei SSc-Betroffenen sollte individuell festgelegt werden, wie häufig Zahnstein und weiche bakterielle Beläge (Plaque/Biofilm) entfernt werden müssen. Bei Zahnverlust sollte auch bei SSc-Erkrankten das Kauorgan funktionell und ästhetisch mit konventionellem festsitzendem und/oder herausnehmbarem Zahnersatz versorgt werden. Die Vor- und Nachteile einer Implantat-chirurgischen und einer prothetischen Versorgung sollten im Rahmen einer interdisziplinären Risiko-Nutzen-Abwägung besprochen werden.
Gastrointestinale Beteiligung
SSc-Erkrankte sollten regelmäßig nach Funktionsstörungen des oberen und unteren Gastrointestinaltraktes befragt werden. Bei Refluxbeschwerden und einer erfolglosen probatorischen Refluxtherapie oder bei Alarmsymptomen soll eine Endoskopie durchgeführt werden. Das Management der Erkrankten mit Hinweisen auf GERD bzw. Dysphagie sollte gemäß der aktuellen Reflux-Leitlinie durchgeführt werden. SSc-Betroffene sollten mittels Gewichtsangaben und eines validierten Instrumentes (z. B. Malnutrition Universal Screening Tool, MUST) auf Mangelernährung gescreent werden.
Nierenbeteiligung
Nierenfunktion (Kreatinin, ggf. Cystatin-C), Urinparameter (Protein-Kreatinin-Ratio) und Blutdruck sollen bei Betroffenen alle 6 Monate kontrolliert werden. Zur Einschätzung einer SSc-assoziierten renalen Krise (SRC) sollte man sich an den Klassifikationskriterien für die hypertensive und normotensive SRC orientieren. Der Blutdruck soll bei Betroffenen und Risikofaktoren für eine SRC zweimal pro Woche kontrolliert werden, bevorzugt als Selbstmessung zu Hause. Bei Blutdruckanstieg um systolisch >30 mmHg bzw. diastolisch >20 mmHg sollte der/die Behandler/in konsultiert werden. Eine GK-Therapie mit >10 mg/Tag Prednisolonäquivalent sollte vermieden werden. Falls dennoch erforderlich, sollte insbesondere bei Vorliegen von weiteren SRC-Risikofaktoren wie RNA Polymerase III-Antikörper und einer Herzbeteiligung, die Nierenfunktion mindestens wöchentlich kontrolliert werden. Betroffene mit arterieller Hypertonie und Proteinurie sollten mit ARB, ggf. in Kombination mit CKB antihypertensiv behandeln werden. Schon bei V. a. eine SRC soll eine Nephrologin/ein Nephrologe frühzeitig hinzugezogen werden und die Behandlung in einem SSc-Zentrum erfolgen.
Eine Nierenbiopsie ist zur Diagnostik der SRC nicht zwingend erforderlich, sollte aber in unklaren Fällen in Erwägung gezogen werden. ACE-Inhibitoren (ACEi) sind die Therapie der Wahl bei der SRC und sollen bis zur maximal tolerablen Dosis rasch gesteigert werden, auch wenn sich die Nierenfunktion hierunter verschlechtert. Bei Intoleranz eines ACEi kann als 2.Wahl ein ARB eingesetzt werden. Bei Zeichen der thrombotischen Mikroangiopathie, insbesondere bei einer ausgeprägten Thrombozytopenie, Zeichen einer TTP oder eines aHUS kann eine Plasmapherese in Erwägung gezogen werden. Die Therapie mit einem ACEi soll trotzdem fortgeführt werden. SSc-Erkrankte mit renaler Krise und mit folgenden Risikofaktoren für eine erhöhte Mortalität sollten intensivmedizinisch überwacht werden: Blutdruck >180/>100 mmHg, zerebraler Krampfanfall, Lungenödem, Tachyarrhythmie, schweres akutes Nierenversagen. Die ACEi-Therapie soll grundsätzlich langfristig nach einer SRC fortgeführt werden, auch bei Eintritt einer dialysepflichtigen Niereninsuffizienz, da sich die Nierenfunktion auch nach Monaten noch erholen kann.
Muskuloskelettale Manifestationen
Sehnenreiben ist bei SSc-Erkrankten mit schweren Organmanifestationen und einer hohen Mortalität assoziiert und sollte systematisch erfasst werden. Eine Physiotherapie und physikalische Therapie sind wichtig für den Erhalt der Funktion und sollen bei allen SSc-Erkrankten mit muskuloskelettalen (MSK)-Manifestationen regelmäßig durchgeführt werden. Die Therapie von MSK-Manifestationen soll erfolgen unter Berücksichtigung aller Organmanifestationen. GK können zur Überbrückung eingesetzt werden, längere Therapien mit >10 mg Prednisolon sollen nicht eingesetzt werden. Bei Arthritis, Tendinitis, Enthesitis und Myopathien soll eine immunmodulierende Therapie durchgeführt werden. Bis zum Wirkungseintritt kann eine überbrückende Therapie mit GK und NSAR, sowie eine GK-Lokaltherapie erfolgen.
Patientenorientierte Parameter und Selbsthilfegruppen
Bei SSc-Erkrankten sollen regelmäßig Lebensqualität, Depressivität und Fatigue erfasst und in einem multimodalen Therapiekonzept berücksichtigt werden. Der Einsatz von validierten Instrumenten kann erwogen werden.
Fertilität, Sexualität und Schwangerschaft
Die Familienplanung soll bereits zu Beginn der SSc-Therapie in das Behandlungskonzept einbezogen werden. SSc-Betroffenen im reproduktionsfähigen Alter sollen vor einer CYC-Therapie fertilitätsprotektive Maßnahmen angeboten werden. Sexuelle Dysfunktion bei Frauen und erektile Dysfunktion bei Männern mit SSc sollten erfasst und bei Vorhandensein interdisziplinär behandelt werden. Bei SSc-Patientinnen mit Kinderwunsch sollte das Vorhandensein von Anti-Phospholipid- und Anti-SSA/SSB-Antikörpern in der Planung berücksichtigt werden. Vor einer Konzeption sollte die Krankheitsaktivität 6-12 Monate unter einer Therapie stabil niedrig sein, die während der Schwangerschaft fortgesetzt werden kann. Schwangerschaften von SSc-Patientinnen sollen als Risiko-Schwangerschaften eingestuft und interdisziplinär betreut werden.
HSCT und andere zelluläre Therapien
Die autologe hämatopoetische Stammzelltransplantation (aHSCT) stellt bei progressiver SSc mit Haut- und Lungenbeteiligung eine etablierte und effektive Therapie für frühe und/oder rapid progressive Verläufe dar. Eine Diskussion dieser Option sollte bei entsprechender Risikokonstellation möglichst früh erfolgen. Eine aHSCT soll nur an Zentren mit ausreichender Erfahrung durchgeführt werden. Derzeit nur im Rahmen von Studien eine Option sind die CAR-T-Zelltherapie oder bispezifische Antikörper.
FAZIT: Eine eingehende Lektüre der Leitlinie ist überaus lohnenswert, da sie teilweise über die EULAR-Empfehlungen hinausgeht bzw. diese ergänzt und beispielsweise stärker die massiv mit der Mortalität assoziierte Herzbeteiligung adressiert oder den patientenrelevanten Zahn-, Mund- und Kieferstatus sowie den Themenkomplex Sexualität, Familienplanung und Risikoschwangerschaften.
https://register.awmf.org/de/leitlinien/detail/060-014
Quelle: Session „DGRh-Leitlinien UpDate 2025“, 19. September 2025