Als Late-breaking Abstract von Iain McInnes, Glasgow (Großbritannien), und Kollegen vorgestellt wurden die 24-Wochen-Ergebnisse der randomisierten, doppelblinden, placebo- und aktiv kontrollierten Phase-III-Studie BE OPTIMAL, in der der IL-17A/F-Inhibitor Bimekizumab über 52 Wochen bei bDMARD-naiven Patienten mit aktver PsA geprüft wurde. Die Studie setzte sich aus einer 16-wöchigen doppelblinden und anschließend 36-wöchigen Therapie-verblindeten Phase zusammen. In die Studie eingeschlossen wurden insgesamt 852 bDMARD-naive Patienten ≥18 Jahre mit aktiver PsA (SJC/TJC je ≥3; mindestens eine aktive psoriatische Läsion und/oder Psoriasis in Anamnese) (im Mittel 48,7 Jahre, BMI 29,2, 46,8 % Männer, Zeit seit Diagnose 5,9 Jahre, SJC/TJC ca. 17/9,5), die im Verhältnis 3:2:1 auf s.c. Bimekizumab 160 mg alle 4 Wochen (Q4W), Placebo oder s.c. Adalimumab 40 mg alle 2 Wochen (Q2W) als Referenz randomisiert wurden; ab Woche 16 wechselten die Placebo-Patienten auf Bimekizumab. Primärer Endpunkt war das ACR50-Ansprechen in Woche 16, sekundäre Endpunkte (hierarchisch) in Woche 16 waren der ΔHAQ-DI, das PASI90-Ansprechen, ΔSF-36 PCS, minimale Krankheitsaktivität (MDA) sowie die radiografische Progression (ΔvdH-mTSS) und die Resolution von Enthesitis (LEI) und Daktylitis (LDI). Bis Woche 16 bzw. 24 blieben 821 (96,4 %) bzw. 806 (94,6 %) der Patienten in der Studie.
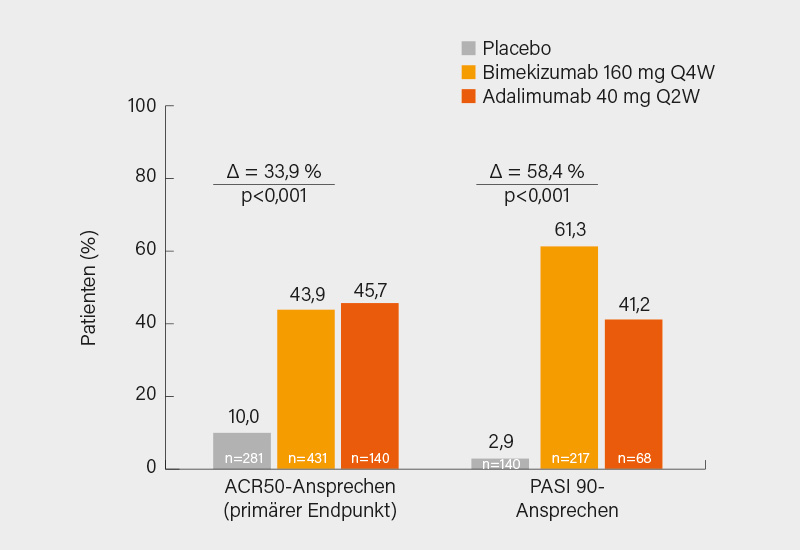
Der primäre Endpunkt ACR50-Ansprechen in Woche 16 wurde signifikant erreicht (43,9 vs. 10,0 %; p<0,001; Adalimumab 45,7 %), ebenso alle hierarchischen sekundären Endpunkte. Noch größer war die Differenz in Woche 16 etwa im PASI 90-Ansprechen (61,3 vs. 2,9 %; p<0,001; Adalimumab 41,2 %) (Abb. 1). Bis Woche 24 erreichten unter Bimekizumab und Adalimumab 65,4/70,7 %, 45,5/47,1 % und 29,2/30,0 % ein ACR20/50/70-Ansprechen, die in Woche 16 auf Bimekizumab umgestellte Patienten holten rasch auf. Ein PASI 75/90/100-Ansprechen in Woche 24 erreichten analog 81,1/58,8 %, 72,8/47,1 % bzw. 56,2/38,2 % der Patienten. Eine MDA wiesen in Woche 16 je 45 % in den Verumarmen und in Woche 24 48,5 bzw. 47,9 % auf. Konsistent wurde eine Hemmung der strukturellen Progression nachgewiesen. Auch die Verträglichkeit war gut (Bimekizumab-assoziierte Candida-Infektionen waren mit 2,6 % selten), alle und schwere unerwünschte Ereignisse (UE) waren ähnlich verteilt. (1)
Bimekizumab vor und nach bDMARDs gleich effektiv
Die randomisierte, doppelblinde, placebokontrollierte Phase-III-Studie BE COMPLETE, in der Bimekizumab bei PsA-Patienten mit unzureichendem Ansprechen auf TNFα-Inhibitoren geprüft wurde, stellten Joseph F. Merola, Boston (USA), und Kollegen vor. In die Studie eingeschlossen wurden 400 Patienten mit aktiver PsA für ≥6 Monate, einem SJC/TJC je ≥3, ≥1 psoriatischen Läsion und/oder Psoriasis in Anamnese sowie Versagen oder Intoleranz von 1-2 TNFα-Inhibitoren (für PsA oder Psoriasis). Die Teilnehmer (im Mittel 50,5 Jahre, BMI 29,8, 47,5 % Männer, Zeit seit Diagnose 9,5 Jahre, SJC/TJC ca. 19/10) wurden für 16 Wochen im Verhältnis 2:1 auf Bimekizumab 160 mg Q4W oder Placebo randomisiert. Der primäre Endpunkt war wiederum das ACR50-Ansprechen in Woche 16, wichtige sekundäre Endpunkte (hierarchisch) waren der ΔHAQ-DI, PASI 90, ΔSF-36 PCS und die MDA. 97 % der Patienten schlossen die 16-wöchige doppelblinde Studienphase ab.
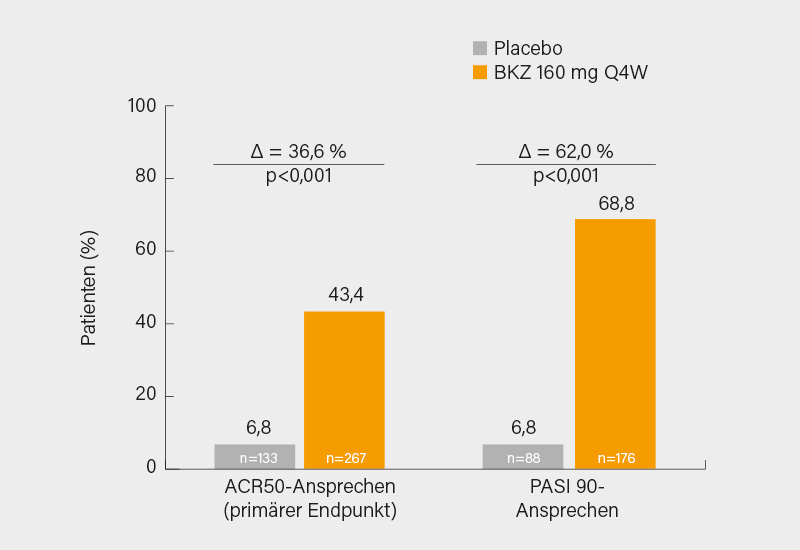
Der primäre Endpunkt wurde mit 43,4 vs. 6,8 % (p<0,001) signifikant erreicht, das ACR50-Ansprechen auf Bimekizumab war somit fast identisch mit jenem in BE-OPTIMAL, obwohl 77 % der Patienten zuvor auf einen TNFα-Inhibitor versagt hatten. Alle hierarchischen sekundären Endpunkte wurden erreicht, so ein PASI 90-Ansprechen in Woche 16 von 68,8 vs. 6,8 % (p<0,001) (Abb. 2). Das ACR20- bzw. ACR70-Kriterium erfüllten 67,0 bzw. 26,6 % der Bimekizumab-Patienten, einen PASI 75 82,4 vs. 10,2 %; eine MDA erreichten 44,2 vs. 6,0 % (p<0,001). Auch bei der körperlichen Funktion zeigten sich signifikante Vorteile für den IL-17A/F-Inhibitor. Wieder zeigte sich ein recht gutes Sicherheitsprofil, therapieassoziierte UE wurden bei 40,1 vs. 33,3 % verzeichnet, eine orale Candidiasis trat erneut bei 2,6 % der Patienten unter Bimekizumab auf. (2)
Zusammengefasst ist sicher von einer Zulassung von Bimekizumab auszugehen, gerade die hohen MDA-Raten stechen hervor. Das Hautansprechen ist exzellent, ob aber bei PsA relevant besser als bei IL-23- oder konventionellen IL-17A-Inhibitoren, das bleibt offen. Beim Gelenkansprechen fanden sich keine Vorteile gegenüber Adalimumab.
Neuer IL-17A-Inhibitor Izokibep überzeugt in Phase-II
Über eine randomisierte, doppelblinde, placebokontrollierte Phase-II-Parallelgruppen– und Dosisfindungsstudie zu Izokibep berichteten Frank Behrens, Frankfurt/M., und Kollegen. In der Studie wurden 135 Patienten mit aktiver psA (SJC/TJC je ≥3) und Versagen auf NSAR oder csDMARD oder TNFα-Inhibitoren im Verhältnis 1:1:1 für 16 Wochen auf Izokibep 40 oder 80 mg Q2W oder Placebo randomisiert (im Mittel 48,5 Jahre, BMI 29,0, SJC/TJC 10 bzw. 17, Krankheitsdauer 7 Jahre, 13 % mit TNF-Versagen, 80 % begleitendes csDMARD). Primärer Endpunkt war das ACR50-Ansprechen von Izokibep 80 mg Q2W versus Placebo, sekundäre Endpunkte waren der ACR20/70, MDA, DAS28, DAPSA, SPARCC, LDI, PASI sowie die Verträglichkeit und Sicherheit.
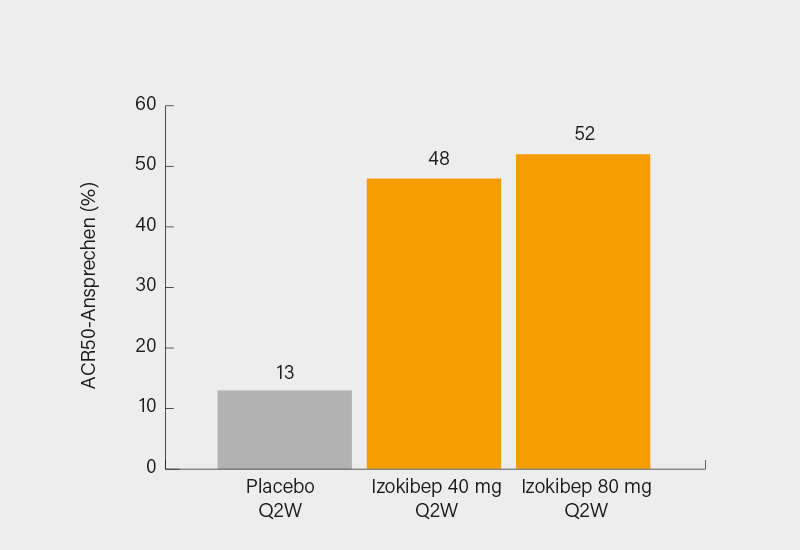
Der primäre Endpunkt wurde signifikant erreicht (p=0,0003) mit einem ACR50 bei 52 und 48 vs. 13 % (80/40 mg/Placebo) der Patienten (Abb. 3). Ein ACR20-Ansprechen erreichten 75 und 60 vs. 26 %, das ACR70-Kriterium erfüllten 20 und 32 vs. 5 %. Ein PASI 75/90-Ansprechen trat bei bis zu 85 bzw. 57 % der Patienten ein, eine vollständige Resolution der Enthesitis (LEI) bei 88 % (80 mg) – letzteres ist besonders bemerkenswert. Auch eine klinisch relevante Verbesserung der Lebensqualität (PsAID-Score) wurde beobachtet (41 und 31 vs. 12 %). Das Sicherheitsprofil war vergleichbar mit jenem der konventionellen IL-17A-Inhibitoren, die Rate von UE bewegte sich auf Placeboniveau. Angesichts des starken Ansprechens von Haut, Gelenken und vor allem Enthesitis wird die Substanz in Phase-III getestet werden, dann womöglich in einer noch höheren Dosierung. (3)
Axiale PsA: Spezifische Charakteristika im Fokus
Ein viel diskutiertes Thema war die axiale PsA. Von den zahlreichen Vorträgen und Abstracts sei hier eine Interimsanalyse der prospektiven deutschen GESPIC Axial PsA-Kohorte von Henriette Käding, Berlin, und Kollegen herausgegriffen. Bei den bislang 88 Patienten mit durch Bildgebung gesicherter axPsA (im Mittel 45 Jahre, 57 % Frauen) zeigte sich ein im Vergleich zu klassischen axSpA-Patienten höherer Anteil betroffener Frauen und seltener eine HLA-B27-Positivität (48 %). Entzündliche Rückenschmerzen lagen bei 77 % vor, eine periphere Beteiligung bei 50 %. Etwa 70 % der Patienten erfüllten sowohl die ASAS- als auch CASPAR-Kriterien. Im MRT fiel bei 17 % eine isolierte Beteiligung der Wirbelsäule auf. Detailliertere Langzeitdaten, die einen Vergleich zu den axSpA-Patienten der GESPIC-Kohorte zulassen, werden in knapp 2 Jahren vorliegen. (4)
Quellen:
1 Ann Rheum Dis 2022; 81(Suppl 1): 206-207 (Abstr. LB0001)
2 Ann Rheum Dis 2022; 81(Suppl 1): 167-169 (Abstr. OP0255)
3 Ann Rheum Dis 2022; 81(Suppl 1): 170-171 (Abstr. OP0258)
4 Ann Rheum Dis 2022; 81(Suppl 1): 19 (Abstr. OP0026)