AXIALE SPONDYLOARTHRITIS
NEUE ASAS-SPARTAN-KLASSIFIKATIONSKRITERIEN ENTHÜLLT
Auf dem ACR-Kongress 2025 wurden die gemeinsam von der Assessment of SpondyloArthritis International Society (ASAS) und dem Spondyloarthritis Research and Treatment Network (SPARTAN) entwickelten, überarbeiteten axSpA-Klassifikationskriterien vorgestellt. Dabei handelt es sich um eine Weiterentwicklung der ASAS-Kriterien aus dem Jahr 2009, deren Nutzen zwar breit anerkannt wurde, die jedoch vor allem aufgrund ihrer begrenzten Spezifität zunehmend kritisch diskutiert wurden. Ziel der Revision war es, die diagnostische Schärfe und Homogenität von Studienpopulationen zu verbessern und so die Aussagekraft klinischer Studien zu erhöhen.
Die Grundlage der Neuentwicklung bildete die internationale CLASSIC-Kohorte, in der Patientinnen und Patienten mit chronischem Rückenschmerz und Verdacht auf axSpA prospektiv und standardisiert untersucht wurden. Das finale Modell basiert auf einem gewichteten Punktesystem, dessen Parameter mithilfe von LASSO-Regressionsanalysen ermittelt wurden. Die Auswahl und Festlegung erfolgte konsentiert im Kreis der ASAS- und SPARTAN-Expertinnen und -Experten.
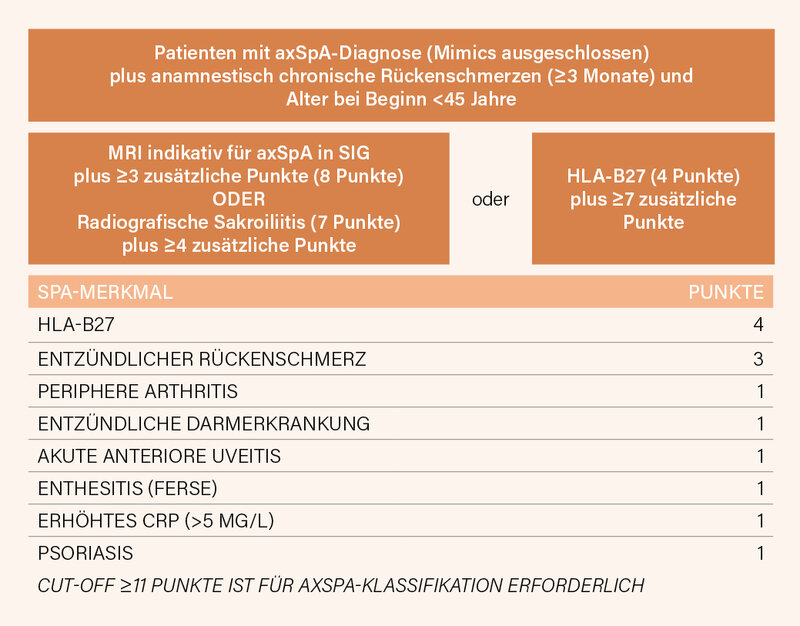
Die neuen Kriterien verlangen zunächst das Vorliegen einer ärztlich gestellten axSpA-Diagnose unter Ausschluss relevanter Differenzialdiagnosen sowie chronischen Rückenschmerz mit Beginn vor dem 45. Lebensjahr. Liegt eine Magnetresonanztomografie (MRT) mit axSpA-typischen Veränderungen der Sakroiliakalgelenke (SIG) vor, sind zusätzlich mindestens 3 Punkte aus dem SpA-Parameterkatalog erforderlich. Alternativ reicht bei röntgenologischer Sakroiliitis eine Mindestpunktzahl von 4. Für Patientinnen und Patienten ohne bildgebenden Nachweis genügt HLA-B27-Positivität in Kombination mit mindestens 7 weiteren Punkten. Insgesamt gilt eine axSpA-Klassifikation als erfüllt, wenn die Summe der SpA-Punkte ≥11 beträgt (Abb. 1). In der Validierungskohorte erreichten die neuen Kriterien eine Sensitivität von 79,5 % und eine Spezifität von 90,4 %. Im Vergleich zur Fassung von 2009 wurde die Zahl der klinischen Variablen reduziert, gleichzeitig wurde die Bildgebung – insbesondere die MRT der Sakroiliakalgelenke – deutlich gestärkt.
Es bleibt zu betonen, dass es sich ausdrücklich um Klassifikations- und nicht um Diagnosekriterien handelt. Für den klinischen Alltag bedeutet das: Die Entscheidung über Diagnose und Therapie muss weiterhin individuell durch erfahrene Rheumatologinnen und Rheumatologen getroffen werden. Patientinnen und Patienten mit milder oder untypischer Verlaufsform, negativem HLA-B27 oder ohne bildgebendem Nachweis könnten durch das neue Schema potenziell nicht klassifiziert werden, obwohl eine axSpA vorliegt. Umgekehrt besteht bei Interpretation unspezifischer MRT- oder Röntgenveränderungen weiterhin das Risiko von Fehlklassifikationen – besonders im Bereich mechanisch-degenerativer Veränderungen. Insgesamt stellen die überarbeiteten ASAS-SPARTAN-Kriterien einen wichtigen Fortschritt für die Klassifikation von axSpA in Forschungskontexten dar. Für die klinische Diagnosestellung bleiben sie jedoch Hilfsmittel unter vielen – die differenzierte Gesamtbeurteilung bleibt auch weiterhin unerlässlich. (1)
WECHSEL DES BIOLOGIKUMS NACH TNF-INHIBITOR-VERSAGEN?
Die ROC-SpA-Studie untersuchte in einem multizentrischen, randomisierten Studiendesign die Wirksamkeit eines Wirkmechanismuswechsels zu einem Interleukin (IL)-17A-Inhibitor im Vergleich zur Zyklisierung mit einem zweiten TNF-Inhibitor bei axSpA-Patientinnen und -Patienten, die auf eine initiale TNF-Inhibitor-Therapie unzureichend angesprochen hatten. Eingeschlossen wurden Personen mit aktiver Erkrankung (Bath Ankylosing Spondylitis Disease Activity Index [BASDAI] >4 oder Axial Spondyloarthritis Disease Activity Score [ASDAS] >3,5) und dokumentiertem primären Therapieversagen nach drei Monaten unter dem ersten TNF-Inhibitor. Die Teilnehmenden erhielten entweder einen IL-17A- oder einen zweiten TNF-Inhibitor, dies bei stabiler Begleitmedikation über mindestens vier Wochen. Primärer Endpunkt war das Erreichen eines ASAS40-Ansprechens nach 24 Wochen.
Die Ergebnisse zeigten keine Überlegenheit der IL-17A-Inhibitor-Gruppe im Vergleich zur zweiten TNF-Inhibitor-Gruppe: Die ASAS40-Ansprechraten betrugen 15,2 % unter einem IL-17A- und 14,5 % unter einem TNF-Inhibitor. Auch bei sekundären Endpunkten wie ASAS20, ASDAS-Verbesserung und ASAS-Teilremission wurden keine signifikanten Unterschiede festgestellt. Der Rückgang der Krankheitsaktivität war in beiden Gruppen vergleichbar. Die Therapietreue bis Woche 54 betrug 62,8 % in der IL-17A- und 54,9 % in der TNF-Inhibitor-Gruppe. Unerwünschte Ereignisse traten ähnlich häufig auf, und es wurden keine neuen Sicherheitssignale identifiziert.
Explorative Trends deuten darauf hin, dass ein IL-17A-Inhibitor potenziell von Vorteil sein könnte bei primärem Nichtansprechen, bei HLA-B27-Negativität, Psoriasis oder niedrigem C-reaktivem Protein (CRP). Wenn hingegen der erste TNF-Inhibitor aufgrund unerwünschter Ereignisse abgesetzt wurde, zeigte sich ein günstigeres Bild für die TNF-Inhibitor-Zyklisierung. Diese Ergebnisse liefern wichtige Erkenntnisse für die Praxis. Sie zeigen, dass ein Wechsel des Wirkmechanismus nach TNF-Versagen nicht grundsätzlich zu besseren Ergebnissen führt als eine Sequenztherapie mit einem zweiten TNF-Inhibitor. Vielmehr unterstützen sie die aktuelle ASAS-EULAR-Empfehlung, bei TNF-Inhibitor-Versagen zwar einen Wechsel zu einem anderen Biologikum zu erwägen, aber ohne, dass ein Wirkmechanismenwechsel zwingend erforderlich ist, insbesondere wenn kein primäres Therapieversagen vorliegt. Die Studie unterstreicht die Notwendigkeit einer individualisierten, gemeinsam mit der Patientin oder dem Patienten getroffenen Therapieentscheidung nach Versagen einer Erstlinientherapie mit TNF-Inhibitor. (2)
PSORIASIS-ARTHRITIS
EFFEKTIVITÄT VON DEUCRAVACITINIB IN EINEM BIOLOGIKA-NAIVEN KOLLEKTIV
In der Phase-III-Studie POETYK PsA-1 wurde die Wirksamkeit und Sicherheit des selektiven oralen TYK-2-Inhibitors Deucravacitinib über 52 Wochen bei Patientinnen und Patienten mit aktiver PsA untersucht, die bisher keine Biologika erhalten hatten. Alle eingeschlossenen Personen erfüllten die CASPAR-Kriterien, wiesen eine aktive Psoriasis oder dokumentierte Psoriasis auf, mindestens drei geschwollene und drei druckschmerzhafte Gelenke (SJC/TJC), ein CRP ≥3 mg/l sowie mindestens eine erosive Veränderung in den Händen oder Füßen im Ausgangsröntgen. 670 Patientinnen und Patienten wurden im Verhältnis 1:1 randomisiert und erhielten entweder Deucravacitinib 6 mg täglich oder Placebo für 16 Wochen. Ab Woche 16 wurde von Placebo auf Deucravacitinib umgestellt.
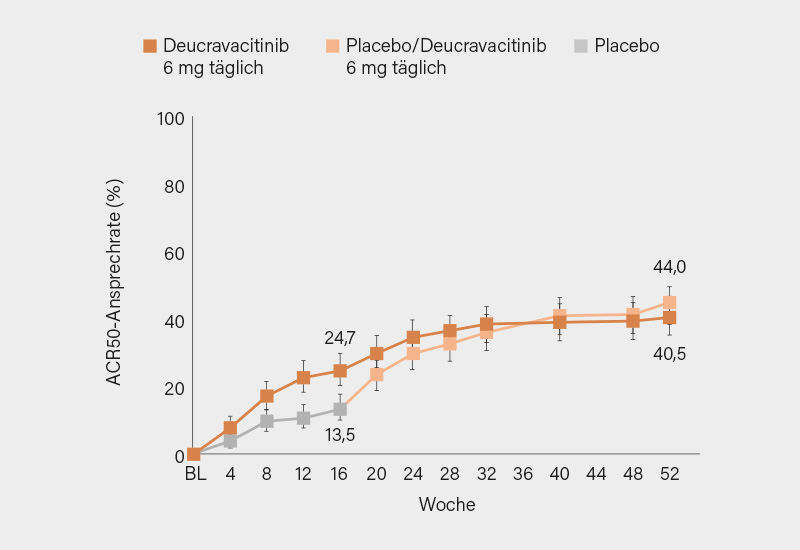
Der primäre Endpunkt (ACR20 in Woche 16) wurde erreicht, mit einem signifikanten Vorteil gegenüber Placebo. Die Ansprechraten für ACR50 (Abb. 2) und ACR70 stiegen weiter bis Woche 24 an und blieben stabil bis Woche 52. Auch patientenberichtete Endpunkte sowie Hautmanifestationen und Enthesitis verbesserten sich unter Deucravacitinib anhaltend. Die Hemmung der radiologischen Progression, bereits in Woche 16 beobachtet, konnte bis Woche 52 bestätigt werden. Patientinnen und Patienten, die initial Placebo erhielten und dann auf Deucravacitinib wechselten, zeigten nach Umstellung eine Reduktion der Progression. Die Behandlung wurde gut vertragen. Es traten nur wenige schwerwiegende Nebenwirkungen und Therapieabbrüche auf. Auch wurden keine neuen Sicherheitssignale beobachtet, insbesondere keine Hinweise auf thromboembolische Ereignisse oder opportunistische Infektionen. Todesfälle traten nicht auf.
Diese Daten belegen die klinische Wirksamkeit von Deucravacitinib über ein Jahr hinweg, sowohl hinsichtlich Gelenk- als auch Hautmanifestationen, und zeigen eine anhaltende Kontrolle der Krankheitsaktivität einschließlich der strukturellen Progression. Das Sicherheitsprofil blieb stabil und steht im Einklang mit vorherigen Studien. (3) Eine Zulassung von Deucravacitinib für die Indikation PsA wird in Bälde erwartet, aktuell ist es lediglich für die Therapie der kutanen Psoriasis zugelassen.
SECUKINUMAB ZEIGT ÜBERLEGENHEIT GEGENÜBER USTEKINUMAB
Die deutsche AgAIN-Studie ist die erste randomisierte, doppelblinde, aktiv-kontrollierte Studie, die den IL-17A-Inhibitor Secukinumab direkt mit dem IL-12/23-Inhibitor Ustekinumab bei Patientinnen und Patienten mit PsA vergleicht, die zuvor auf TNF-Inhibitoren unzureichend angesprochen hatten oder diese nicht vertrugen. Insgesamt wurden 119 Teilnehmende an 28 rheumatologischen Zentren in Deutschland eingeschlossen und im Verhältnis 1:1 randomisiert. Die Studienpopulation war durch hohe Krankheitslast und Therapieresistenz gekennzeichnet, rund zwei Drittel hatten zuvor Adalimumab erhalten. Trotz vorzeitigem Rekrutierungsstopp wurde die Studie erfolgreich abgeschlossen.
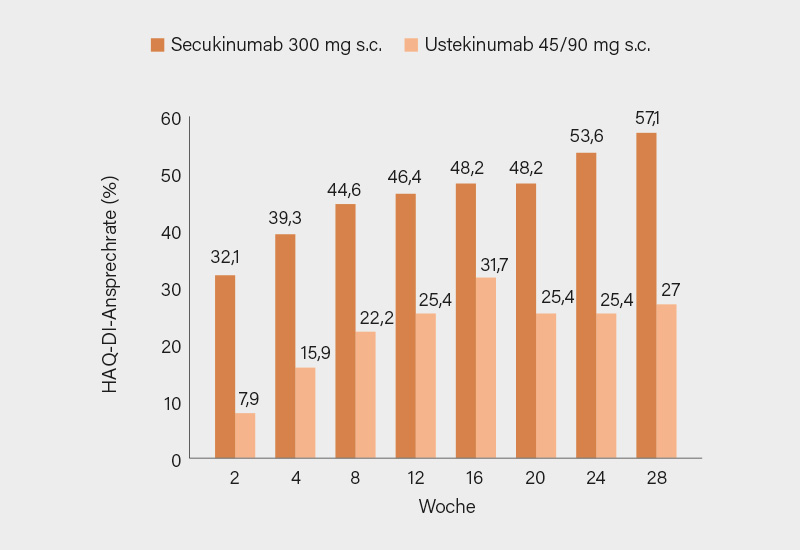
Der primäre Endpunkt – eine Verbesserung des Health Assessment Questionnaire – Disability Index (HAQ-DI) – wurde in der Secukinumab-Gruppe in deutlich höherem Ausmaß erreicht als in der Ustekinumab-Gruppe: 57,1 % der mit dem IL-17A-Inhibitor behandelten Patientinnen und Patienten erreichten eine klinisch relevante Verbesserung im HAQ-DI, gegenüber 27,0 % unter Ustekinumab (Odds Ratio, OR 3,65; 95% KI 1,60–8,31; p=0,002) nach 28 Wochen Therapie (Abb. 3). Auch in allen sekundären und explorativen Endpunkten zeigte sich ein konsistenter Vorteil zugunsten von Secukinumab – einschließlich Gelenkbefall, Hautmanifestationen, Schmerz und patientenberichteten Outcomes. Die Verbesserungen traten früh auf (bereits ab Woche 2) und hielten bis Woche 28 an. Die Verträglichkeit beider Substanzen war insgesamt gut. Unerwünschte Ereignisse traten in beiden Gruppen häufig, aber überwiegend mild auf. Neue Sicherheitssignale wurden unter keiner der beiden Therapien festgestellt.
Die Ergebnisse der AgAIN-Studie liefern erstmals Head-to-Head-Daten zu Secukinumab im Vergleich zu Ustekinumab in einem TNF-Inhibitor-erfahrenen PsA-Kollektiv und zeigen eine deutliche Wirksamkeitsüberlegenheit von Secukinumab in dieser Patientinnen- und Patienten-Gruppe. (4) Es bleibt jedoch offen, ob ein vergleichbarer Vorteil auch gegenüber einem modernen IL-23-Inhibitor wie Guselkumab oder Risankizumab nachweisbar gewesen wäre.
EINFLUSS VON ÜBERGEWICHT UND ADIPOSITAS AUF THERAPIEANSPRECHEN
In einer longitudinalen Kohortenstudie wurde untersucht, wie sich ein erhöhter Body-Mass-Index (BMI) auf das Erreichen von minimaler Krankheitsaktivität (MDA) bei PsA-Patientinnen und -Patienten auswirkt. Die Analyse basierte auf Daten aus einem großen, seit 1978 prospektiv geführten PsA-Kollektiv, in dem Patientinnen und Patienten alle sechs Monate standardisiert dokumentiert werden. Die Auswertung umfasste 1.291 Betroffene mit verfügbaren BMI-Werten. Der mittlere BMI lag bei 28,8 kg/m², das Durchschnittsalter bei 44,9 Jahren, 55 % waren Männer. Insgesamt erhielten 428 Teilnehmende eine fortgeschrittene Therapie, darunter TNF-, IL-17-, IL-12/23-, IL-23- und JAK-Inhibitoren sowie den Phosphodiesterase (PDE)-4-Inhibitor Apremilast.
Ein höherer BMI war mit einer signifikant geringeren Wahrscheinlichkeit assoziiert, eine MDA zu erreichen (OR 0,95; 95% KI 0,94-0,97), insbesondere hinsichtlich subjektiver Komponenten wie Schmerz, Globalbeurteilung, Enthesitis, Hautbefall und funktioneller Einschränkung. Kein signifikanter Zusammenhang bestand hingegen mit der Anzahl geschwollener Gelenke. Die Ergebnisse blieben auch nach Adjustierung für Kovariablen wie Alter, Geschlecht, Komorbiditäten, Rauchstatus und radiografische Schäden in multivariaten Modellen bestehen. Subgruppenanalysen zeigten, dass der negative Effekt eines erhöhten BMI auf das Erreichen von MDA insbesondere unter TNF-Inhibitoren ausgeprägt war (OR 0,93; 95% KI 0,89-0,97).
Diese Ergebnisse unterstreichen die klinische Bedeutung von Adipositas als negativer Prädiktor für das Therapieansprechen bei PsA. Da sich der Einfluss überwiegend auf subjektive und hautbezogene Endpunkte konzentriert, könnten neben der systemischen Inflammation auch psychosoziale Faktoren und die Schmerzverarbeitung eine wichtige Rolle spielen. (5)
GLP-1-REZEPTORAGONISTEN MIT VORTEILHAFTEN EFFEKTEN
In einer ebenfalls kanadischen, retrospektiven Analyse zweier PsA-Kohorten wurde untersucht, welchen Einfluss GLP-1-Rezeptoragonisten wie Semaglutid, Liraglutid und Tirzepatid auf das Gewicht, die Krankheitsaktivität und metabolische Parameter bei Patientinnen und Patienten mit PsA haben. Die 48 eingeschlossenen Teilnehmenden (60 % weiblich, mittleres Alter 52,7 Jahre, medianer BMI 34,9 kg/m²) wiesen häufig multiple Komorbiditäten auf: 65 % waren adipös, 35 % hatten Diabetes, die Mehrheit litt an mindestens drei Begleiterkrankungen.
Nach Einleitung der Therapie mit einem GLP-1-Rezeptoragonisten kam es zu einem signifikanten mittleren Gewichtsverlust von 6,4 kg. Entzündungsparameter wie das CRP sowie Schmerzen und Triglyzeride gingen signifikant zurück. Die Disease Activity in Psoriatic Arthritis (DAPSA)-Scores und die globale Einschätzung der Patientinnen und Patienten zeigten numerische Verbesserungen, erreichten jedoch keine statistische Signifikanz. In linearen Regressionsmodellen war der prozentuale Gewichtsverlust signifikant mit Verbesserungen bei DAPSA, Schmerz, Lipoprotein niedriger Dichte (LDL)-Werten, systolischem Blutdruck und EQ-5D-Werten assoziiert. Eine Reduktion des Körpergewichts um 1 % war mit einem Rückgang des DAPSA um 0,49 Punkte verbunden.
Diese Real-World-Daten deuten darauf hin, dass GLP-1-Rezeptoragonisten in der Versorgung von PsA-Patientinnen und -Patienten mit metabolischen Risikofaktoren ein therapeutisches Potenzial über die reine Gewichtskontrolle hinaus haben. Die beobachteten Verbesserungen in Schmerz, Entzündung und metabolischen Parametern waren proportional zum Ausmaß der Gewichtsreduktion. (6) Prospektive kontrollierte Studien sind erforderlich, um die Rolle von GLP-1-Rezeptoragonisten als komplementärer Therapieansatz bei PsA zu klären – dies insbesondere auch bei nicht-adipösen Patientinnen und Patienten.
Prof. Dr. med. Denis Poddubnyy
Division of Rheumatology, Department of Medicine,
University Health Network and University of Toronto, Toronto, Kanada
Med. Klinik m. S. Gastroenterologie, Infektiologie und Rheumatologie, Charité – Universitätsmedizin Berlin
Quellen:
1 Maksymowych W et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 0854
2 Dalix E et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB09
3 van der Heijde D et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB20
4 Behrens F et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. LB06
5 Mehta P et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2691
6 Eder L et al., Arthritis Rheumatol 2025; 77(Suppl 9): Abstr. 2687