Die Empfehlungen, die aufgrund ihrer deutlich stärkeren Fokussierung auf die individuell vorliegenden PsA-Manifestation von vielen Rheumatologen gegenüber jenen der EULAR favorisiert werden, gelten für erwachsene Psoriasis- und PsA-Patienten und basieren auf einem systematischen Durchforsten von Datenbanken (MEDLINE, EMBASE und Cochrane CENTRAL), das seit der letzen Fassung bis ins Jahr 2020 durchgeführt wurde. Zudem wurden Kongresspräsentationen bis 2020 berücksichtigt. Unter Anwendung der GRACE-Methodologie mit systematischen Literaturreviews wurden zunächst sieben konsentierte „Overarching Principles“ sowie grundsätzliche Empfehlungen für das Management der PsA-Manifestationen sowie damit assoziierten Erkrankungen (Uveitis, chronisch-entzündliche Darmerkrankungen [CED]) ausgesprochen. Auch Empfehlungen zum Management von Komorbiditäten wurden integriert, da diese oft die Wahl der Therapie beeinflussen. Überdies wurden sog. „Position Statements“ zu Biosimilars und zum Therapieabbau eingeführt.
Die wichtigste Aussage: Die Wahl der Therapie für einen einzelnen Patienten sollte idealerweise alle Bereiche abdecken, die sich auf diesen auswirken, und die gemeinsame Entscheidungsfindung unterstützen. So fordert ein neues „Overarching principle“, dass Therapien um patientenspezifische Domänen zentriert werden sollten mit speziellem Augenmerk auf eine „shared decision“ von Arzt und Patient. Die frühere Domäne der Komorbiditäten wurde unterteilt in Uveitis, CED und andere Komorbidiäten. Geblieben ist es bei den Kategorien periphere Arthritis (DMARD-naiv oder IR-, bDMARD-IR), axiale Arthritis (bDMARD-naiv oder –IR), Enthesitis, Daktylits, Psoriasis und Nagelpsoriaisis. IL-17, -23 und JAK-Inhibitoren(i) wurden in mehreren Kategorien aufgewertet. Die Empfehlungen für den PDE-4i Apremilast wurden auf Enthesitis, Daktylitis und Nagelpsoriasis ausgeweitet.
Übergreifende Prinzipien und Position Statements
Zunächst in geraffter Form zu den übergreifenden Prinzipien. Die ultimativen Ziele der PsA-Therapie bestehen a) im Erreichen einer möglichst niedrigen Krankheitsaktivität in allen Domären, b) der Optimierung des funktionellen Status und c) der Vermeidung/Minimierung von Komplikationen. Die Untersuchung von PsA-Patienten bedarf der Berücksichtigung aller Domären (inkl. Uveitis, CED), der Einfluss von Schmerzen, Funktion, Lebensqualität und von strukturellen Schäden sollte erfasst werden. Zur klinischen Untersuchung zählen im Idealfall PROs, eine umfassende Anamnese und körperliche Untersuchung, Labor und Bildgebung (z. B. Röntgen, Sonografie, MRT) sowie die Nutzung akzeptierter Scores. Komorbiditäten (z. B. Adipositas, metabolisches Syndrom, kardiovaskuläre Erkrankungen, Depression/Angst, Lebererkrankungen, chronische Infektionen, Malignitäten, Osteoporose, Fibromyalgie) oder andere Aspekte (Schwangerschaft) sollten berücksichtigt werden, eine multidisziplinäre Betreuung kann hier Vorteile haben. Therapieentscheidungen sollten individualisiert sein und von Arzt/Patient gemeinsam getragen werden („shared decison making“). Ferner wird aufgrund der Vorteile einer frühen Diagnose/Therapie eine möglichst sofortige Evaluation und Behandlung (inkl. Überweisung an Spezialisten) empfohlen.
Nicht näher eingegangen sei auf die Statements zu Biosimilars. Zum Therapieabbau wird festgehalten, dass dieser bei Patienten in Remission/niedriger Krankheitsaktivität erwogen werden kann, wieder in enger Abstimmung mit den Patienten. Mögliche Schübe oder potenzielle Probleme, nach dem Tapering wieder eine gute Krankheitskontrolle zu erreichen sind zu kommunizieren, der Einfluss auf andere Outcomes (z. B. kardiovaskuläres Risiko) sollte bedacht werden.
Spezifische Therapieempfehlungen
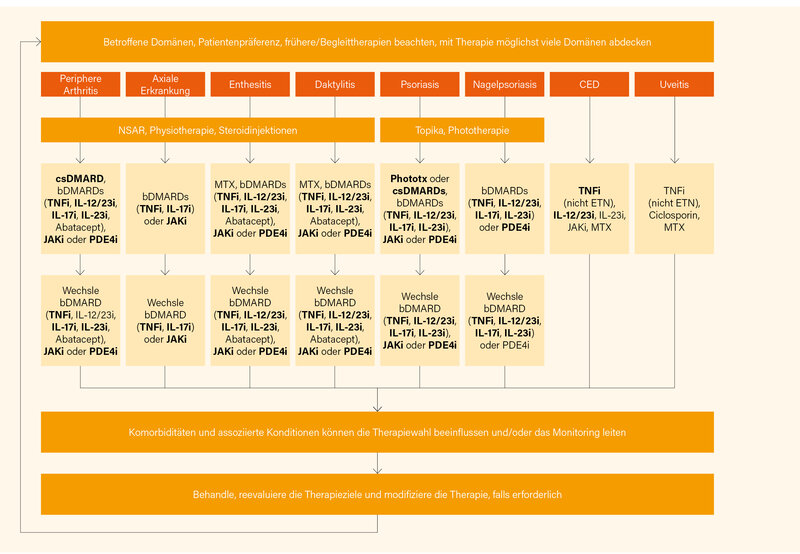
Bei peripherer Arthritis (DMARD-naiv) gibt es starke Empfehlungen für csDMARDs (außer Ciclosprin), TNFi, IL-12/23i, IL-17i, IL-23, JAKi und PDE4i, nur bedingt für NSAR, orale oder i.a. Glukokortikoide (GK). Bei DMARD-IR-Patienten gibt es eine starke Empfehlung für alle b/tsDMARDs (inkl. Apremilast), nur eine bedingte für Abatacept. Bei bDMARD-erfahrenen Patienten gibt es eine starke Empfehlung für einen Wechsel auf TNFi, IL-17i, IL-23i oder JAKi, etwas schwächer werden Ustekinumab, Abatacept und Apremilast gewertet. Bei axialer Erkrankung (bDMARD-naiv) gibt es eine starke Empfehlung für NSAR, Analgetika, Physiotherapie, TNFi, IL-17i, IL-23i oder JAKi, von PDE4i und csDMARDs wird abgeraten, für IL-12/23i und IL-23i wurde auf eine Empfehlung verzichtet (für IL-23i ist dies eigentlich schon wieder überholt). Erste Wahl bei Enthesitis und Daktylitis sind TNFi, IL-12/23i, IL-17i, IL-23i, JAKi und PDE4i, nur bedingt empfohlen werden NSAR, MTX und Abatacept (sowie ggf. GK-Injektionen). Bei Psoriasis werden topische/Phototherapien, MTX, Fumarsäure/ester, Ciclosporin sowie TNFi, IL-12/23i, IL-17i, IL-23i, PDE4i und JAKi stark empfohlen (je nach Schwere), bedingt auch Acitretin. Bei Nagelpsoriasis gibt es starke Empfehlungen für TNFi, IL-12/23i, IL-17i, IL-23i und PDE4i, nur bedingt für JAKi, csDMARDs und andere Therapien. Im Falle von CED (Morbus Crohn, Colitis ulcerosa) werden jeweils TNFi (außer Etanercept) und IL-12/23i stark, IL-23i, JAKi und MTX bedingt empfohlen. Von IL-17i wird explizit abgeraten. Bei Uveitis gibt eine bedingte Empfehlung für TNFi (außer Etanercept), Ciclosporin und MTX. Die Details der möglichen Abfolge sind einem Therapiealgorithmus (Abb.) zu entnehmen.
Was ist bei Komorbiditäten zu beachten?
Aufgrund des erhöhten kardiovaskulären Risikos wird ein Screening auf Risikofaktoren empfohlen, bei Adipositas (negativ mit Funktion und Krankheitsaktivität assoziiert) wird eine Gewichtsreduktion angeraten, bei Fettleber ein Monitoring der Leberwerte. Es sollte ferner vor Therapiebeginn ein Screening auf aktive Hepatitis B und C sowie HIV und eine latente Tuberkulose erfolgen. Zu denken ist an ein erhöhtes Herpes Zoster-Risiko v. a. unter JAKi, eine Impfung sollte möglich vor Therapiestart erfolgen. Aufgrund des erhöhten Risikos für Hautkrebs wird eine jährliche Hautuntersuchung empfohlen. Zu beachten sind natürlich auch Osteoporose und Fibromyalgie. Gehäuft ist bei PsA mit Depression/Angst zu rechnen (oft mit schlechtem Outcome assoziiert), daher ist an ein Screening sowie (bei Verdacht) die Überweisung zur Diagnose und psychologische Unterstützung zu denken.
Der Originalarbeit ist eine hilfreiche Tabelle zu Therapien zu entnehmen, die bei diesen Komorbiditäten nicht oder nur mit Vorsicht eingesetzt werden sollten.
Quelle: Nat Rev Rheumatol 2022;
doi: 10.1038/s41584-022-00798-0