Zunächst zur EGPA, bei der orale GK und Immunsuppressiva (IS) weiterhin die Basis der Standardversorgung (SoC) darstellen. Ihr Langzeitgebrauch ist allerdings mit unerwünschten Ereignissen assoziiert und auch Rezidive sind relativ häufig. In der multizentrischen, 52-wöchigen, randomisierten, doppelblinden, aktiv-kontrollierten Parallelgruppen-Phase-III-Nichtunterlegenheitsstudie MANDARA wurde bei EGPA-Patienten auf SoC die Effektivität und Sicherheit von Benralizumab und dem IL-5-Inhibitor Mepolizumab (das einzige für EGPA zugelassene Medikament) untersucht bzw. verglichen. In die Studie eingeschlossen wurden 140 erwachsene Patienten (im Mittel 52,3 Jahre, 60 % Frauen) mit dokumentierter EGPA basierend auf Asthma und Eosinophilie plus ≥2 weiteren EGPA-Merkmalen und anamnestisch rezidivierender/refraktärer Erkrankung, die eine stabile Therapie mit oralen GK (≥7,5 mg/Tag) mit/ohne stabile immunsuppressive Therapie für ≥4 Wochen vor Randomisierung erforderte. Im Verhältnis 1:1 wurden die Patienten auf s.c. Benralizumab 1x 30 mg oder Mepolizumab 3x 100 mg alle 4 Wochen für 52 Wochen randomisiert, orale GK wurden nach erreichter Krankheitskontrolle reduziert. Primärer Endpunkt war der Anteil von Patienten in Remission (definiert als Birmingham Vasculitis Activity Score [BVAS] =0 und GK-Dosis ≤4 mg/Tag) sowohl in Woche 36 als auch Woche 48.
Benralizumab auf dem Weg zur EGPA-Zulassung
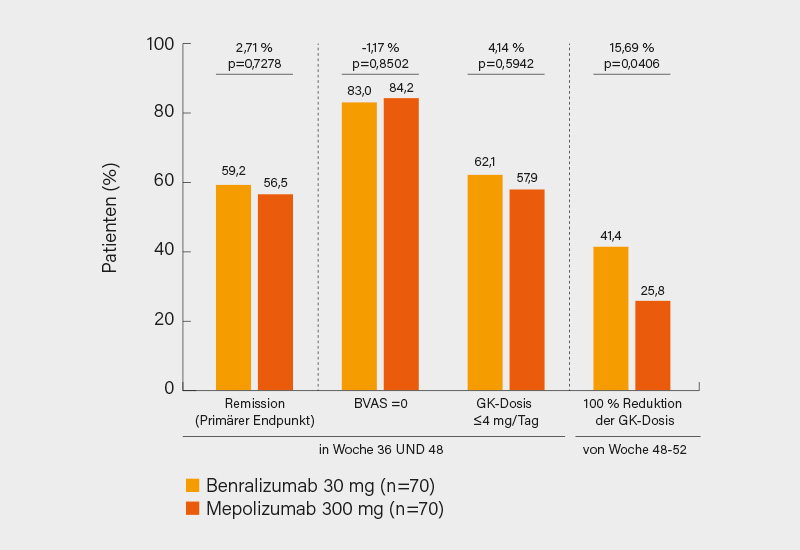
Im Ergebnis betrug die adjustierte Remissionsrate zu sowohl Woche 36 als auch 48 59,2 % unter Benralizumab im Vergleich zu 56,5 % unter Mepolizumab (Δ 2,71 %, 95% KI -12,54 bis 17,96; p=0,7278), die Nichtunterlegenheit von Benralizumab gegenüber Mepolizumab (bei einer vordefinierten Marge von -25 %) bestätigend. Einen isolierten BVAS =0 erreichten 83,0 vs. 84,2 %, eine GK-Dosis ≤4 mg/Tag 62,1 vs. 57,9 % der Patienten. Im Hinblick auf eine 100 %-Reduktion der GK-Dosis (initial betrug diese 11 mg/Tag) von Woche 48-52 zeigte sich sogar ein signifikanter Vorteil von Benralizumab (41,4 vs. 25,8 %; p=0,041) (Abb.), etwas häufiger gelang auch eine Reduktion um ≥50 % (86,1 vs. 73,9 %). Bezüglich sekundärer Endpunkte wie erreichte und anhaltende Remission, Steroidbedarf oder klinischer Nutzen zeigten sich jeweils vergleichbare Raten. Die Rezidivrate betrug in beiden Gruppen 30 %. Zu unerwünschten Ereignissen (UE) kam es bei 90,0 % der Patienten unter Benralizumab im Vergleich zu 95,7 % unter Mepolizumab, meist handelte es sich um COVID-19 (21,4 vs. 27,1 %), Kopfschmerzen (17,1 vs. 15,7 %) und Arthralgien (17,1 vs. 11,4 %). Schwerwiegende UE wurden bei 5,7 vs. 12,9 % der Teilnehmer beobachtet, nur bei 2 Mepolizumab-Patienten führten diese zum Therapieabbruch. Die Nichtunterlegenheit von Benralizumab versus Mepolizumab (in Kombination mit SoC) in puncto Remission einschließlich eines häufiger erreichten völligem Absetzen von GK bei rezidivierender/refraktärer EGPA wurde somit bei guter Verträglichkeit bestätigt, einer Zulassung dürfte (außer der formal fehlenden „echten“ Placebogruppe) nichts im Wege stehen. (1)
Wie sicher ist das PEXIVAS-Regime im Praxisalltag?
Auch bei schwerer Granulomatose mit Polyangiitis (GPA) und mikroskopischer Polyangiitis (MPA) sind (in Kombination mit Rituximab [RTX] oder Cyclophosphamid [CYC]) GK Basis der Therapie. In der PEXIVAS-Studie war die Nichtunterlegenheit eines dosisreduzierten GK-Regimes in puncto Tod und terminale Niereninsuffizienz (ESRD) bei weniger schweren Infektionen belegt worden. Jedoch beinhaltete der primäre Endpunkt nicht Progress oder Rezidive und es wurde zumeist CYC zur Remissionsinduktion eingesetzt – in der Subgruppe mit RTX gab es einen Trend für ein erhöhtes Risiko von Tod oder ESRD. Eine retrospektive multizentrische Studie verglich nun das PEXIVAS- (53,8 %) mit dem GK-Standardregime (46,2 %) bei 234 Patienten mit schwerer GPA (n=148) und MPA (n=93). Primärer Endpunkt waren Tod, ESRD und Progression vor Remission (mit Therapieintensivierung) oder Rezidiv, diesen erreichten binnen 12 Monaten 26,5 % der Patienten, 33,3 % unter dem PEXIVAS- vs. 18,5 % unter dem Standardregime (p=0,016).
In einer multivariaten Analyse war das reduzierte GK-Regime signifikant mit dem primären Endpunkt assoziiert (Hazard Ratio, HR 1,72; 95% KI 1,08-2,74), nicht jedoch mit einem erhöhten Risiko für Tod oder ESRD (HR 1,62; 95% KI 0,82-3,19). Es gab keine signifikante Differenz bei schweren Infektionen nach einem Jahr (20,6 vs. 15,7 %, p=0,427). Nach Propensity Score-Matching war die reduzierte GK-Dosis im Trend mit einem häufigeren Erreichen des primären Endpunkts verbunden (HR 1.57; 95% KI 0,93-2,64). Patienten der Subgruppe auf dem PEXIVAS-Regime mit Kreatinin-Spiegeln >300 mmol/l erreichten öfter den primären Endpunkt (Rate Ratio, RR 2,14; 95% KI 1,14-4,03). Dasselbe galt für die mit RTX behandelte Subgruppe (HR 1,61; 95% KI 0,94-2,77), die auch ein höheres Risiko für Tod oder ESRD aufwies (HR 2,42; 95% KI 1,04-5,66). Vor allem bei Patienten mit hohen Kreatinin-Spiegeln oder mit RTX als Induktionstherapie muss somit mit einem erhöhten Risiko unter dem GK-dosisreduzierten PEXIVAS-Regime gerechnet werden. (2)
Mit Statin gegen Atherosklerose-Progression bei AAV?
Nur kurz erwähnt sei eine ebenfalls von Benjamin Terrier, Paris (Frankreich), und Kollegen vorgestellte randomisierte, doppelblinde, placebokontrollierte Phase-III-Studie, in der eine Primärprävention schwerer kardiovaskulärer Ereignisse (MACE) mit Rosuvastatin 20 mg/Tag bei 111 AAV-Patienten (55 % Männer, im Mittel 55 Jahre) in Remission über 24 Monate untersucht wurde mit der Carotis-Intima-Media-Dicke (cIMD) als subklinischem Marker für Atherosklerose (und damit das subsequente MACE-Risiko). Im primären Endpunkt, der cIMD-Veränderung über 24 Monate, zeigte sich ebenso wenig eine signifikante Differenz (p=0,89) wie bezüglich der Anzahl von Plaques (p=0,94); nur der LDL-Cholesterin- und hsCRP-Spiegel wurden unter dem Statin jeweils signifikant gesenkt. (3)
Quellen:
1 ACR Convergence 2023; Late Breaking-Poster L14
2 Arthritis Rheumatol 2023; 75 (Suppl 9): Abstr. 0725
3 Arthritis Rheumatol 2023; 75 (Suppl 9): Abstr. 0858