In die multizentrische, retrospektive Studie im Rahmen des nationalen französischen VEXAS-Studienregisters wurden zwischen November 2020 und August 2023 insgesamt 110 Patienten mit genetisch nachgewiesenem VEXAS-Syndrom eingeschlossen (99 % Männer, medianes Alter 71 Jahre), die ≥1 zielgerichtete Therapie erhalten hatten. Ein vollständiges Ansprechen (CR) war definiert als ein Komposit aus klinischer Remission, CRP <10 mg/l und Glukokortikoid (GK)-Dosis <10 mg/Tag, ein partielles Ansprechens (PR) beinhaltete eine klinische Remission sowie die Reduktion von CRP und GK-Therapie um 50 %. Das Kriterium eines Nicht-Ansprechens war bei persistierender klinischer Aktivität und/oder biologischem Entzündungssyndrom und/oder Unfähigkeit, die GK-Dosis zu reduzieren, erfüllt.
Keine Wirksamkeit von anderen Biologika nachweisbar
Zu den eingesetzten Therapien zählten Januskinase-Inhibitoren (JAKi) bei 40 % der Patienten (n=78, Ruxolitinib in 87 % der Fälle), Interleukin-6-Rezeptorinhibitoren (IL-6Ri) bei 26 % (n=51, Tocilizumab zu 92 %), IL-1-Inhibitoren (IL-1i) bei 17 % (n=33, Anakinra zu 91 %), TNFα-Inhibitoren (TNFi) in 10 % (n=20) und andere zielgerichtete Therapien bei 6 % (n=12). 53 Patienten (48 %) erhielten ≥1 zielgerichtete Therapie (insgesamt waren es 194). Die wesentlichen klinischen Merkmale des VEXAS-Syndroms bei Initiierung der „targeted“-Therapie waren konstitutionelle Symptome (82 %), Hautbeteiligung (76 %) und entzündliche Arthralgien (60 %). Ein myelodysplastisches Syndrom lag in 28 % der Fälle vor, aber ohne Indikation für eine spezifische hämatologische Behandlung. Der mediane CRP-Spiegel zu Therapiebeginn betrug 39 (19-57) mg/l, die mediane Prednison-Dosis 20 (10-35) mg/Tag.
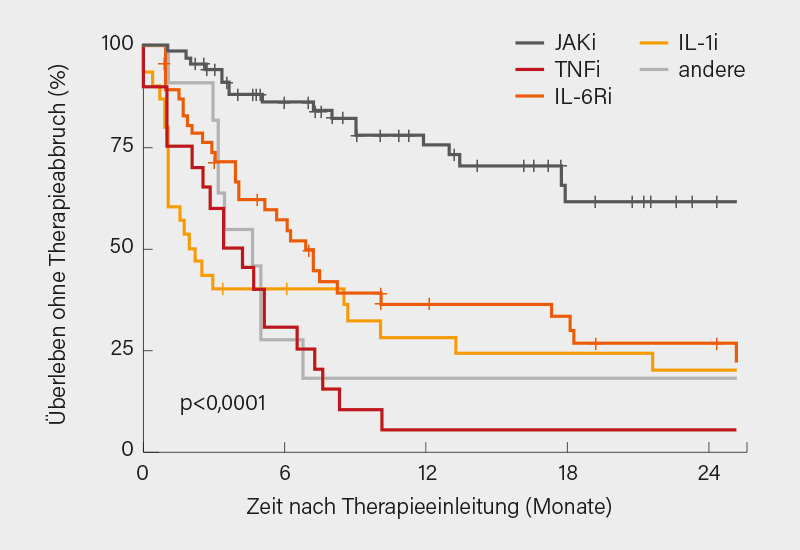
Nach 3 Monaten betrug das Gesamtansprechen (CR und PR) 24 % (CR 19 % und PR 5 %) unter JAKi, 32 % (CR 20 % and PR 12 %) unter IL-6Ri, 9 % unter IL-1i und 0 % unter TNFi oder anderen zielgerichteten Therapien. Zu Monat 6 belief sich das Gesamtansprechen auf 30 % (CR 26 % und PR 4 %) unter JAKi und 26 % (CR 20 % und PR 6 %) unter IL-6Ri. Ein Entzug von GK gelang unter JAKi und IL-6Ri ähnlich häufig. Im Vergleich zu JAKi waren die anderen Therapien mit einem signifikant höheren Risiko für ein Absetzen der Behandlung während des Follow-up verbunden (p<0,001) (Abb.). Die Therapie wurde abgesetzt in 28 % der Fälle (n=22) unter JAKi nach median 7,2 (3,4-12,4) Monaten und in 69 % der Fälle unter IL-6Ri nach median 5,1 (2,0-9,1) Monaten. Die Gründe für einen Therapieabbruch bestanden in einem primären Versagen (43 %), sekundären Versagen (14 %), schweren unerwünschten Ereignissen (19 %) oder Tod (19 %) unter JAKi, die entsprechenden Raten unter IL-6Ri betrugen 46, 11, 31 und 9 %, unter IL-1i 50, 4, 35 und 8 % sowie 74, 5, 16 und 5 % unter TNFi.
In dieser ersten größeren Studie zum Vergleich zielgerichteter Therapien bei Patienten mit VEXAS-Syndrom bestätigten sich die (in kleinen Fallserien) ermittelten Vorteile von JAKi und Tocilizumab mit ungefähr vergleichbaren Ansprechraten, aber längerem Therapieverbleib auf JAKi (primär Ruxolitinib). Doch auch darunter ist bei 70 % der Betroffenen kein dauerhafter Nutzen zu erzielen. Andere Therapien, vor allem TNFi, scheinen ineffektiv zu sein – für genauere Aussagen bedarf es aber prospektiver Therapiestudien.
Quelle: ACR Convergence 2023, Late-breaking Poster L03