COVID-19 führt zu einer raschen Aktivierung des angeborenen Immunsystems in Form erhöhter Spiegel proinflammatorischer Effektor-Zytokine wie TNF, Interleukin (IL)-1b, IL-6, IL-8, G-CSF und GM-CSF (Granulozyten-[Monozyten]-Kolonie-stimulierender Faktor) sowie Chemokinen wie MCP1, IP10 und MIP1a, insbesondere bei kritisch erkrankten Patienten. Zusätzlich sind T Zell-abgeleitete Zytokine wie z. B. IL-17 im Rahmen einer SARS-CoV-2-Infektion erhöht. Bei manchen COVID-19-Patienten entwickelt sich ferner ein Zytokinsturm, der an eine sekundäre hämophagozytische Lymphohistiozytose erinnert, einen durch virale Infektionen angestoßenen hyperinflammatorischen Zustand, berichten die Erlanger Experten.
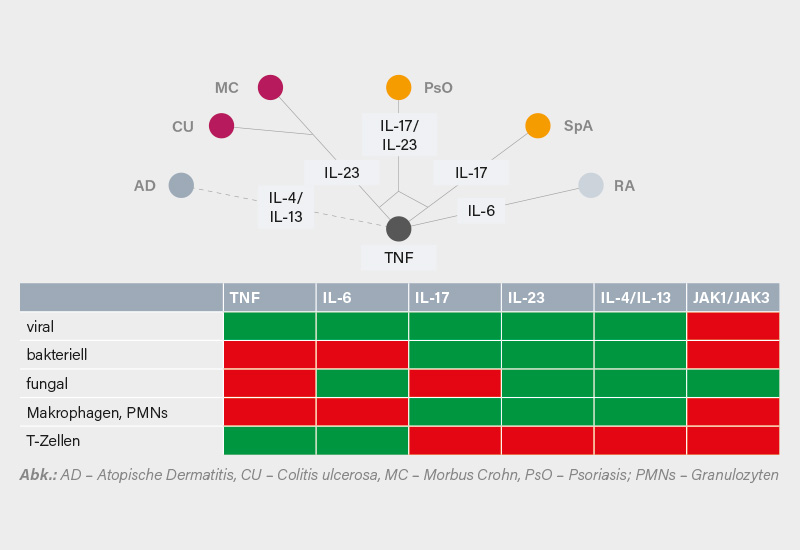
Obwohl die meisten durch SARS-CoV-2 induzierten und bei IMIDs eingesetzten Zytokine eine wichtige Rolle für das Entzündungsgeschehen spielen, scheinen sie nicht essenziell für die Kontrolle der Viruselimination zu sein. So steigern an IL-23 und IL-4/IL-13 ansetzende Therapien nicht das Risiko viraler, bakterieller oder Pilzinfektionen, während die IL-17A-Inhibition lediglich ein Signal für Candida-, nicht aber virale Infektionen zeigt. Anti-TNF und -IL-6-Therapien erhöhen das Risiko bakterieller Infektionen, haben aber geringere Effekte auf virale Infektionen (Ausnahme: Hepatitis B) (Abb.). Obwohl die Inzidenz von Influenza und damit assoziierten Komplikationen z. B. bei RA erhöht ist, fand sich kein solches Signal für Zytokin-Inhibitoren. Auch erreichen mit TNFa-Blockern behandelte RA-Patienten ein normales Immunansprechen nach einer Influenza-Impfung. Die Viruselimination scheint primär von anderen Zytokinen wie IL-15, Typ I-Interferonen und IFNgabzuhängen, so die Autoren.
Obgleich die Zytokin-Inhibition auf den ersten Blick als „Immunsuppression“ zu betrachten ist und insofern schädlich im Kontext der COVID-19-Pandemie, neutralisieren diese Antikörper anderserseits eher spezifische Mediatoren der Entzündungskaskade als dass sie zu einer breiten Immunsuppression führen würden.
Überdies könnten Zytokin-Inhibitoren im Falle eines schweren COVID-19-Verlaufs eine Hyperinflammation abschwächen, weshalb derzeit hierzu auch mehrere Studien zu IL-6R- und IL-6-Inhibitoren (Sarilumab, Tocilizumab) laufen. Etwas anders ist möglicherweise die Situation, wenn anstatt einzelner Zytokine (TNF, IL-6, IL-17A, IL-23 oder IL-4/IL-13), die im Gegensatz zu Glukokortikoiden nicht die Rate viraler Infektionen oder einen schwereren Verlauf von diesen zu fördern scheinen, wie im Falle von JAK-Inhibitoren mehrere Zytokine, die auch an Interferon ansetzen, ins Visier genommen werden.
So erhöhen JAK-1- und JAK-3-Inhibitoren bekanntlich das Risiko für Herpes zoster. Diese Angriffspunkte (JAK-1/-3) beeinflussen die Funktion verschiedener Zytokine, die am antiviralen Ansprechen beteiligt sind, wie z. B. Typ I-Interferone, IL-2, IL-15, IL-21 und IFNg. Somit könnten JAK-1/-3-Inhibitoren theoretisch die Elimination von SARS-CoV-2 hemmen. Auf der anderen Seite scheint die JAK-2-Inhibition den Eintritt von SARS-CoV-2-Viren und die IL-17-induzierte Zytokin-Aktivierung zu hemmen. Da IL-6 und GM-CSF, die beide von SARS-CoV-2 induziert werden, partiell oder komplett in den JAK-2-Signalweg involviert sind, ist es nicht überraschend, dass JAK-2 als Angriffspunkt in der Therapie einer Hyperinflammation bei COVID-19 diskutiert und auch in klinischen Studien mit Baricitinib evaluiert wird.
Fazit
Trotz noch unklarer Datenlage scheinen Zytokin-Inhibitoren, die auch gemäß den DGRh-Handlungsempfehlungen im Rahmen der Pandemie nicht abgesetzt werden sollen, nicht per se das Risiko für virale Infektionen oder einen schweren COVID-19-Verlauf zu erhöhen und könnten sich im Gegenteil sogar als effektive COVID-19-Therapien entpuppen.
Quelle: Nat Rev Immunol 2020; 20(5): 271-272