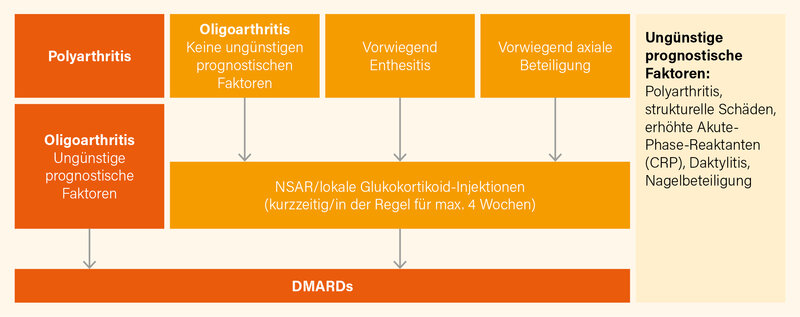
Zunächst zu den EULAR-Empfehlungen für die Therapie der PsA. Bei den übergreifenden Prinzipien wurde eine neue Empfehlung ausgesprochen, die Sicherheitsaspekte der individuellen Therapie zu berücksichtigen, um das Nutzen-Risiko-Verhältnis zu optimieren. Diese Empfehlung wurde sicherlich durch die aktuelle Diskussion rund um die Sicherheit von JAK-Inhibitoren inspiriert. Die neue Leitlinie hat zudem, ähnlich wie bei den GRAPPA-Empfehlungen, ein phänotypbasiertes Vorgehen implementiert (Abb. 1).
PsA: Update der EULAR-Empfehlungen
Die Rolle von NSAR wurde herabgestuft: Die Leitlinie empfiehlt deren Einsatz nur bei Patienten mit Oligoarthritis ohne ungünstige Prognosefaktoren sowie bei Patienten mit Enthesitis und axialen Manifestationen. Des Weiteren wurden die systemischen Glukokortikoide vollständig aus den Empfehlungen entfernt.
Bei Patienten mit Polyarthritis sowie bei Oligoarthritis und Vorliegen von ungünstigen Prognosefaktoren sollte ein csDMARD initiiert werden, vorzugsweise Methotrexat, wenn eine relevante Hautbeteiligung vorliegt. Nach dem Versagen von mindestens einem csDMARD wird ein bDMARD empfohlen, und zwar aus den Gruppen der TNF-, IL-17- bzw. IL-23-Inhibitoren. JAK-Inhibitoren werden erst danach empfohlen oder in Situationen, in denen eine bDMARD-Therapie nicht angemessen ist. Bei Patienten mit Enthesitis werden die bDMARDs (und im nächsten Schritt auch die JAK-Inhibitoren) direkt nach NSAR/lokalen Glukokortikoiden empfohlen. Das Gleiche gilt auch für die axialen Manifestationen, allerdings werden hier die IL-23-Inhibitoren nicht explizit empfohlen. Auch die extra-muskuloskelettalen Manifestationen sind bei der Wahl der Therapie relevant. Bei klinisch relevanter Hautbeteiligung werden IL-17- bzw. IL-23-Inhibitoren empfohlen, bei Uveitis monoklonale Antikörper gegen TNF und bei chronisch-entzündlichen Darmerkrankungen (CED) TNF-, IL-23- bzw. JAK-Inhibitoren. (1)
Extra-muskuloskelettale Manifestationen unter JAK-Inhibition
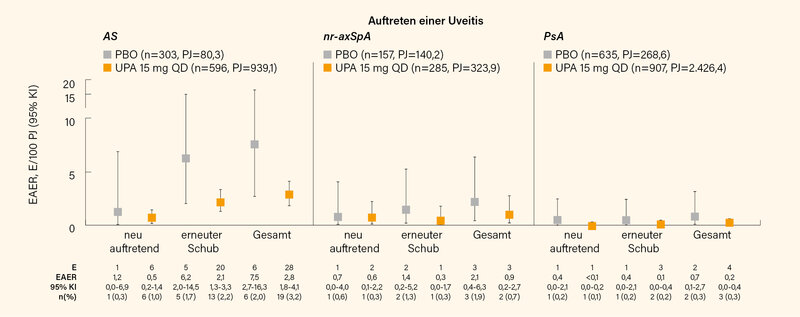
Die extra-muskuloskelettalen Manifestationen der PsA und axSpA spielen eine wichtige Rolle bei der Wahl der Therapie, wie die aktuellen Leitlinien (EULAR, GRAPPA für die PsA, ASAS-EULAR für die axSpA) zeigen. Für die JAK-Inhibitoren liegen positive Daten für die Wirksamkeit bei CED und Psoriasis vor, die Lage bei der Uveitis war bis jetzt ziemlich unklar. In Mailand wurden gepoolte Daten aus Zulassungsstudien mit Upadacitinib (UPA, ein JAK-1 Inhibitor) bei der PsA und bei der axSpA (einschließlich ankylosierender Spondylitis [AS] und nicht-röntgenologischer [nr]-axSpA) präsentiert. Die Analyse umfasste Sicherheitsdaten aus UPA-Studien zur PsA (2 Studien), AS (2 Studien) und nr-axSpA (1 Studie). Alle Studien wurden mit einer anfänglichen Randomisierung zu UPA oder Placebo (PBO) für eine vordefinierte Anzahl von Wochen entworfen, gefolgt von einer offenen Verlängerung, bei der die mit PBO behandelten Patienten auf UPA umgestellt wurden. Behandlungsbedingte unerwünschte Ereignisse (TEAEs) von systemischen Ereignissen wurden bewertet, darunter Uveitis, CED und Psoriasis. TEAEs wurden definiert als ein unerwünschtes Ereignis mit Beginn ab der ersten Dosis des Studienmedikaments und ≤30 Tage nach der letzten Dosis. Das Auftreten von Ereignissen wurde adjustiert für die Dauer der Behandlung berichtet (exposure-adjusted event rates – EAER; Ereignisse/100 Patientenjahre [E/100 PJ]) und nach Patienten mit einer berichteten Vorgeschichte (Schub) der jeweiligen Manifestation und solchen ohne Vorgeschichte (Neuauftreten) stratifiziert.
Bezogen auf Uveitis waren EAER unter Upadacitinib seltener als unter Placebo, die galt sowohl für Schübe als auch für die neu aufgetretene Manifestation. Dabei hatten Patienten mit AS das größte Risiko, eine Uveitis zu entwickeln verglichen mit der nr-axSpA bzw. mit der PsA (Abb. 2). Diese Art der Erfassung (als unerwünschte Ereignisse) ist zwar suboptimal (verglichen mit der systematischen Erfassung von extra-muskuloskelettalem Manifestationen), liefert aber dennoch wichtige Hinweise dafür, dass die JAK-Inhibition durchaus eine positive Auswirkung auf die Häufigkeit von Uveitis-Schüben bei SpA-Patienten haben kann. Eine prospektive Studie mit dem Fokus auf Uveitis wäre dennoch wünschenswert. (2)
axSpA: Head-to-Head Studie: IL-17- vs. TNF-Inhibition
Auf dem Kongress wurden ausführlich die Daten aus SURPASS diskutiert, eine Phase-IIIb-Studie, in der bDMARD-naive Patienten mit aktiver röntgenologischer axSpA (r-axSpA = AS) und Risikofaktoren für die röntgenologische Progression in der Wirbelsäule (hsCRP ≥5 mg/L oder ≥1 Syndesmophyt auf dem Röntgenbild) 1:1:1 zu Secukinumab (SEC, 150/300 mg; verblindete Dosis) oder zu einem Adalimumab-Biosimilar (SDZ-ADL, 40 mg; offene Anwendung) randomisiert wurden. Die Röntgenaufnahmen und MRTs wurden von 3 unabhängigen zentralen Readern gelesen, verblindet für die Behandlung und Chronologie der Bilder. Der primäre Endpunkt war der Anteil der Patienten ohne röntgenologische Progression (Veränderung von Ausgangswert [change from baseline, CFB] im modifizierten Stoke AS Spinal Score [mSASSS] ≤0,5) unter SEC im Vergleich zu SDZ-ADL nach 104 Wochen. Sekundäre Endpunkte waren der CFB-mSASSS nach 104 Wochen, der Anteil der Patienten mit ≥1 Syndesmophyt(en) zum Ausgangszeitpunkt, bei denen keine neuen Syndesmophyt(en) nach 104 Wochen auftraten, die Veränderung in den MRT-Scores für aktive Entzündung und Sicherheit.
Insgesamt wurden 859 Patienten randomisiert: SEC 150 mg (n=287), 300 mg (n=286) oder SDZ-ADL (n=286). Nach 104 Wochen betrug der Anteil der Patienten ohne radiografische Progression 66,1 %, 66,9 % und 65,6 % (p=n.s.), während der mittlere CFB-mSASSS unter SEC 150 mg, 300 mg und SDZ-ADL 0,54, 0,55 bzw. 0,72 betrug. 56,9 %, 53,8 % bzw. 53,3 % der Patienten unter SEC 150 mg, 300 mg bzw. SDZ-ADL mit ≥1 Syndesmophyt(en) zum Ausgangszeitpunkt entwickelten keine neuen Syndesmophyt(en) bis zur 104. Woche. Beide Medikamente konnten die MRT-Entzündung in den Sakroiliakalgelenken (SIG) und in der Wirbelsäule reduzieren. (3)
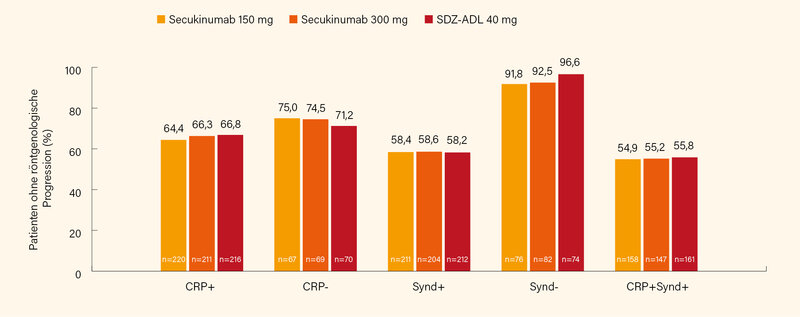
In der nachfolgenden Analyse wurden Patienten nach Risikofaktoren für die röntgenologische Progression (Syndesmophyten, CRP) stratifiziert. Die Syndesmophyten-negative (Synd-) Untergruppe zeigte die geringste Progression in allen röntgenologischen Endpunkten (höherer Anteil an Patienten ohne radiografische Progression und ohne neue Syndesmophyten sowie geringere mittlere Veränderung im CFB-mSASSS), unabhängig vom Behandlungsarm. Die CRP+Synd+-Subgruppe zeigte im Vergleich zu den Synd+- und CRP+-Subgruppen eine höhere radiografische Progression, während die CRP- und Synd--Subgruppen die geringste Progression aufwiesen (Abb. 3). (4)
Validierungsstudie für die ASAS-Klassifikationskriterien für axSpA
Auf dem EULAR-Kongress wurden erstmalig die langersehnten Ergebnisse der CLASSIC (CLassification of Axial SpondyloarthritiS Inception Cohort)-Studie – einem gemeinsamen Projekt von ASAS (Assessment of Spondyloarthritis International Society) und SPARTAN (Spondyloarthritis Research and Treatment Network) – präsentiert. Das Gesamtstudienkonzept folgte einem ähnlichen Format wie bei der Entwicklung der ASAS-Klassifikationskriterien für axiale SpA. Die prospektive Kohorte bestand aus allen aufeinanderfolgenden Patienten, die mit aktuellem und unklarem Rückenschmerz von ≥3 Monaten Dauer und einem Krankheitsbeginn im Alter von ≤45 Jahren an einen Rheumatologen überwiesen wurden. Die Stichprobengröße war mit 500 Teilnehmern aus Nordamerika (SPARTAN-Teil) und 500 aus anderen Teilen der Welt außerhalb Nordamerikas (ASAS-Teil) berechnet. Röntgen- und MRT-Bilder der SIG von allen Patienten wurden durch zentrale erfahrene Reader bewertet. Die finale Diagnose (axSpA bzw. keine axSpA) durch den Rheumatologen unter Berücksichtigung von zentralen bildgebenden Ergebnissen (sowie von sonstigen klinischen und Laborparametern) war der Hauptendpunkt. Das Hauptziel der Studie bestand darin, die ASAS-Klassifikationskriterien von 2009 zu evaluieren. Die Kriterien würden als validiert gelten, wenn sie eine Spezifität von mindestens 90 % und eine Sensitivität von mindestens 75 % aufweisen. Andernfalls müssten die Kriterien entsprechend angepasst werden.
Insgesamt wurden 1.015 Teilnehmer in die Studie eingeschlossen und evaluiert. Die axSpA-Diagnose wurde bei 370 Patienten (36,5 %) gestellt. Die Sensitivität der 2009 ASAS-Klassifikationskriterien betrug in der Kohorte 73,8 %, die Spezifität 84,3 %. Somit wurden die vordefinierten Werte nicht erreicht und die Kriterien sollen im nächsten Schritt angepasst und von beiden Gesellschaften (ASAS und SPARTAN) verabschiedet werden. (5)
Prof. Dr. med. Denis Poddubnyy
Leiter der Rheumatologie am Campus Benjamin Franklin
Medizinische Klinik für Gastroenterologie, Infektiologie und Rheumatologie
Charité – Universitätsmedizin Berlin
Hindenburgdamm 30, 12203 Berlin
Quellen: 1 Gossec L et al., EULAR 2023, EULAR recommendations for the management of psoriatic arthritis: 2023 update – EULAR Recommendations session, 3. Juni 2023 | 2 Poddubnyy D et al., Ann Rheum Dis 2023; 82 (Suppl 1): 40 (OP0061) | 3 Baraliakos X et al., Ann Rheum Dis 2023; 82 (Suppl 1): 38 (OP0059) | 4 Baraliakos X et al., Ann Rheum Dis 2023; 82 (Suppl 1): 882 (POS1115) | 5 EULAR 2023, Session „The Conundrum of diagnosing Axial Spondyloarthritis resolved“, Referenten: R. Landewé, W. Maksymowych, M. Rudwaleit, 3. June 2023