Auch in einer anderen Session wurde die systemische Sklerose (SSc) diskutiert, diesmal mit dem Fokus auf die Therapie der SSc-assoziierten interstitiellen Lungenerkrankung (SSc-ILD), dem wichtigsten Treiber der krankheitsspezifischen Mortalität. Entscheidend bei SSc-ILD scheint die Kombination aus früher antientzündlicher und antifibrotischer Therapie zu sein.
Laut Prof. Dr. Gabriele Riemekasten, Lübeck, sind sowohl die Haut- als auch Lungenfibrose prinzipiell reversibel, wie Studien zur autologen Stammzelltransplantation (ASCT) zeigen. In den meisten Fällen ist aber – gerade bei SSc-ILD – eine Stabilisierung das realistischere Therapieziel. Generell geht die Entzündung der Fibrose voraus, spielt aber auch im Verlauf eine Rolle, sodass bei SSc-ILD sowohl antientzündliche (möglichst eine B-Zell-depletierende Strategie beinhaltend) als auch antifibrotische Therapien gefragt sind.
Antientzündliche Therapien: Update zu Rituximab und Tocilizumab
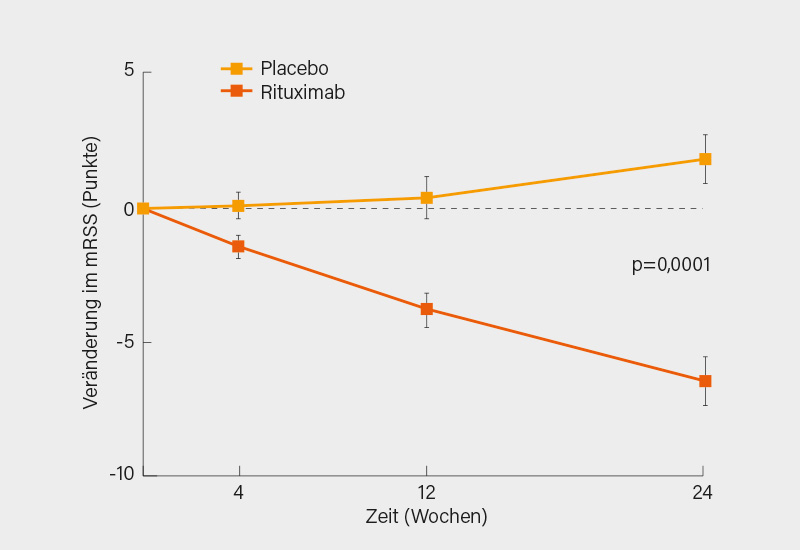
Immunsuppressiva der Wahl sind bei progressiver ILD und stark progressiver Hautfibrose Cyclophosphamid (CYC), eine Alternative stellt (speziell bei ILD) Mycophenolat Mofetil (MMF) dar. Bei refraktären Patienten stellt die Kombination aus MMF und Rituximab eine weitere Option dar, mit gutem Ansprechen der Hautfibrose (mRSS) und Lungenfunktion (FVC). Inzwischen gibt es aus der ersten randomisierten placebokontrollierten Studie DESIRES zu Rituximab bei SSc (keine weiteren Immunsuppressiva, max. 10 mg/Tag Prednison) den Nachweis einer gegenüber Placebo starken Wirksamkeit auf die Haut (nach 24 Wochen ΔmRSS 8,4; p<0,001; Abb.), und auch die FVC stabilisierte sich (p=0,044). In einer prospektiven, offenen Studie zum Vergleich mehrerer Monotherapien schnitt Rituximab in puncto FVC fast so gut ab wie CYC und besser als MMF. Ein ähnliches Bild ergab eine systematische Metaanalyse, generell ließ sich die DLCO durch diese Therapien schlechter beeinflussen als die FVC. Insgesamt ist zu konstatieren, dass die Evidenz für den Nutzen von Rituximab bei SSc deutlich zugenommen hat.
Eine weitere interessante Therapieoption wäre die Interleukin (IL)-6-Rezeptorinhibition mit Tocilizumab. Leider ist die Phase-III-Studie focuSSced formal gescheitert, da der primäre Endpunkt (mRSS) wie zuvor schon in Phase-II verfehlt wurde. Erneut zeigte sich aber eine Stabilisierung der Lungenfunktion, die sich (in einem allerdings anderen Patientenkollektiv) sogar mit den Ergebnissen des antifibrotischen Multi-Tyrosinkinase-Inhibitors Nintedanib messen lassen kann. Zumindest bis Woche 48 war in einer Subgruppe von Patienten mit SSc-ILD der FVC-Verlust unter Tocilizumab nur minimal. Langfristig (Woche 96) stabilisierte oder verbesserte Tocilizumab die Lungenfunktion bei mehr als der Hälfte der Patienten, mit womöglich besonders gutem Effekt bei Patienten mit Anti-Scl70-Antikörpern. In den USA wurde Tocilizumab inzwischen in der Indikation SSc-ILD zugelassen.
Antifibrotische Therapien: Nintedanib vorerst einzige Option
Auf die antifibrotisch wirksamen Therapien bei SSc ging in der Folge Prof. Dr. Jörg Distler, Erlangen, ein. Einen Durchbruch bei SSc-ILD markierte die Zulassung von Nintedanib als erster zielgerichtet antfibrotischer Therapie. Die Grundlage hierfür hatte die Phase-III-Studie SENSCIS gelegt, in der Nintedanib im Vergleich zu Placebo nach 52 Wochen zu einer signifikanten Reduktion der Abnahme der Lungenfunktion um 44 % (FVC-Verlust -52,4 vs. 93,3 ml/Jahr, ΔFVC -41 ml/Jahr; p=0,04) führte. Die höchste Wirksamkeit wurde dabei in Kombination mit MMF erreicht.
In Zukunft könnte sich die antifibrotische Therapie aber wandeln und im Vergleich zum relativ breit wirksamen Nintedanib spezifischer werden. So konnten mittels RNA-Sequenzierung bereits funktionell heterogene Fibroblastenpopulationen identifiziert werden. Eine selektive Inhibition nur der pathogenetisch relevanten Populationen wäre ein vielversprechender Ansatz, der aber derzeit noch Zukunftsmusik ist.
Quelle: Session „Neue Behandlungsstrategien der Systemischen Sklerose“, DGRh-Kongress, 17. September 2021