Das Leitlinien-Update wurde von einer 27-köpfigen interdisziplinären Task Force aus 16 europäischen Ländern und den USA gemäß den üblichen EULAR SOPs basierend auf einer systematischen Literaturrecherche erstellt. Erstmals wurden vier übergreifende Prinzipien formuliert. Alles in Allem gibt es nun 17 spezifische Empfehlungen, 6 Empfehlungen sind neu, 8 wurden überarbeitet, 3 blieben unverändert und 3 wurden in übergreifende Prinzipien umgewandelt. Trotz zahlreicher Fortschritte blieben viele Fragen noch offen, wie auch die umfangreiche „Research Agenda“ unterstreicht, keine Empfehlungen wurden in Bezug auf COVID-19 ausgesprochen, verständlich angesichts der sich ständig ändernden Datenlage.
Erstes übergreifendes Prinzip ist, dass AAV-Patienten die beste Versorgung angeboten werden sollte, die auf einer gemeinsamen Entscheidungsfindung („shared decision“) von Patient und Arzt unter Berücksichtigung von Effektivität, Sicherheit und Kosten basieren muss. Zweitens sollten Patienten Zugang zu Schulung haben mit einem Fokus auf die Auswirkungen von AAV und deren Prognose, wichtigen Warnzeichen und Therapien (inkl. therapieassoziierten Komplikationen). Drittens sollten AAV-Patienten regelmäßig auf therapieassoziierte unerwünschte Ereignisse und Komorbiditäten gescreent werden. Es werden eine Prophylaxe und Lebensstilberatung zur Reduktion therapieassoziierter Komplikationen und anderer Komorbiditäten empfohlen. Viertens wird betont, dass es sich bei AAV um seltene, heterogene und potenziell auch Lebens- und organbedrohende Erkrankungen handelt, die daher eines multidisziplinären Managements in Zentren mit, oder mit sofortigem Zugang zu spezifischer vaskulitischer Expertise bedürfen.
Die wichtigsten Empfehlungen im Überblick
Unverändert ist Empfehlung (1): Eine Gewebebiopsie unterstützt stark die Diagnose einer Vaskulitis und wird zusätzlich empfohlen zur Etablierung einer neuen AAV-Diagnose und zur weiteren Evaluation von Patienten mit Verdacht auf eine rezidivierende Vaskulitis. Neu ist Empfehlung (2): In Patienten mit Zeichen/Symptomen, die den Verdacht auf die Diagnose einer AAV aufkommen lassen, wird eine Testung auf sowohl PR3- als auch MPO-ANCA mit einem qualitativ hochwertigen Antigen-spezifischen Assay als primärem Testverfahren empfohlen. Revidiert wurde Empfehlung (3): Für die Remissionsinduktion von Patienten mit neuer oder rezidivierender, Organ- oder lebensbedrohender GPA/MPA wird die Kombination aus Glukokortikoiden (GK) mit entweder Rituximab (RTX) oder Cyclophosphamid (CYC) empfohlen, bei rezidivierender Erkrankung präferenziell RTX. Modifiziert wurde auch die Empfehlung (4): Für die Remissionsinduktion bei nicht-Organ- oder nicht-lebensdrohender GPA/MPA wird die Kombination aus GK und RTX empfohlen, die in der vorherigen Version noch primär empfohlenen Substanzen Methotrexat (MTX) und Mycophenolat Mofetil (MMF) können als Alternativen zu RTX erwogen werden. Neu ist Empfehlung (5): Als Teil des Regimes zur Remissionsinduktion bei GPA/MPA wird eine orale GK-Therapie empfohlen mit einer Startdosis von 50-75 mg Prednisolon/Tag, in Abhängigkeit vom Körpergewicht. Weiter wird eine schrittweise Reduktion der GK-Dosis auf 5 mg Prednisolon/Tag nach 4-5 Monaten empfohlen (letzteres basierend auf dem Protokoll der PEXIVAS-Studie). Ebenfalls neu ist Empfehlung (6): Avacopan in Kombination mit RTX oder CYC kann zur Remissionsinduktion bei GPA/MPA als Teil einer Strategie zur substanziellen Reduktion der GK-Exposition erwogen werden (dies auf Basis der ADVOCATE-Studie). Revidiert wurde – erneut als Ergebnis der PEXIVAS-Studie – die Empfehlung (7): Ein Plasmaaustausch kann als Teil einer Therapie zur Remissionsinduktion bei GPA/MPA bei Patienten mit Serum-Kreatinin >300 mmol/l aufgrund einer aktiven Glomerulonephritis erwogen werden. Hingegen wird von einer routinemäßigen Anwendung eines Plasmaaustauschs zur Behandlung einer alveolären Hämorrhagie bei GPA/MPA abgeraten. Umformuliert wurde auch Empfehlung (8): Für im Hinblick auf die Remissionsinduktion therapierefraktäre GPA/MPA-Patienten wird eine eingehende erneute Bestimmung des Krankheitsstatus und von Komorbiditäten mit der Erörterung von zusätzlichen oder anderen Therapieoptionen empfohlen. Diese Patienten sollten in enger Abstimmung mit einem Vaskulitis-Zentrum behandelt oder an ein solches überwiesen werden.
Eine Revision erhielten auch die Empfehlungen zur Remissionserhaltung: So wird (9) zur Erhaltung der Remission bei GPA/MPA nach einer Induktion mit entweder RTX oder CYC eine Therapie mit RTX empfohlen. Als Alternativen können Azathioprin oder MTX erwogen werden. Es wird zudem in (10) empfohlen, die remissionserhaltende Therapie bei de-novo GPA/MPA über 24-48 Monate (ab erreichter Remission) fortzuführen. Eine längere Dauer sollte bei rezidivierenden Patienten oder solchen mit erhöhtem Rezidivrisiko erwogen werden, dies aber unter Berücksichtigung der Patientenpräferenz und der Risiken einer fortgesetzten Immunsuppression.
Nun zur EGPA (11): Zur Remissionsinduktion von Patienten mit neuer oder rezidivierender, Organ- oder lebensbedrohender EGPA wird neu eine Kombination aus hochdosierten GK und CYC empfohlen. Eine Kombination aus Hochdosis-GK und RTX kann als Alternative erwogen werden. Auch neu ist Empfehlung (12), wonach für die Remissionsinduktion bei nicht-Organ- oder nicht-lebensdrohender EGPA zu einer Therapie mit GK geraten wird. Bei Patienten (13) mit rezidivierender oder refraktärer EGPA ohne eine aktive Organ- oder lebensbedrohende Erkrankung wird – auf Basis der MIRRA-Studie – neu der Einsatz von Mepolizumab empfohlen. Für die (14) Remissionserhaltung bei EGPA nach erfolgreicher Remissionsinduktion bei Organ- oder lebensbedrohender Erkrankung sollte eine Therapie mit MTX, Azathioprin, Mepolizumab oder RTX erwogen werden. Im Falle einer nicht Organ- oder lebensbedrohenden EGPA wird zur Remissionserhaltung Mepolizumab empfohlen.
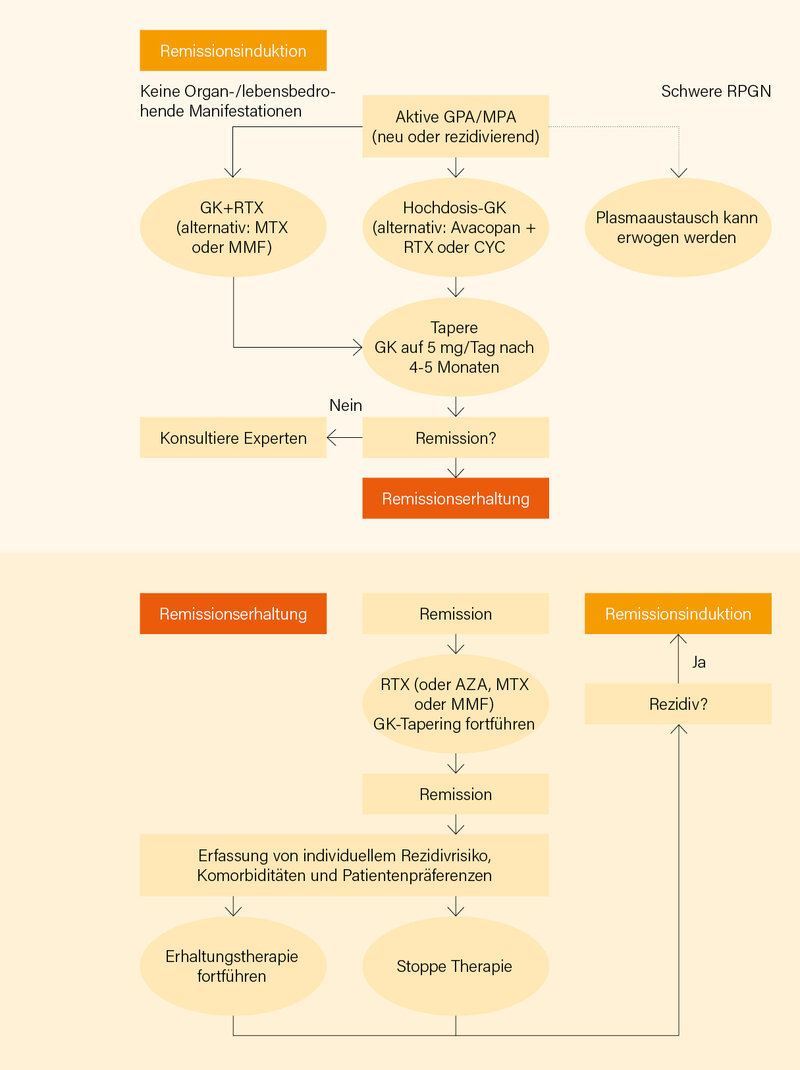
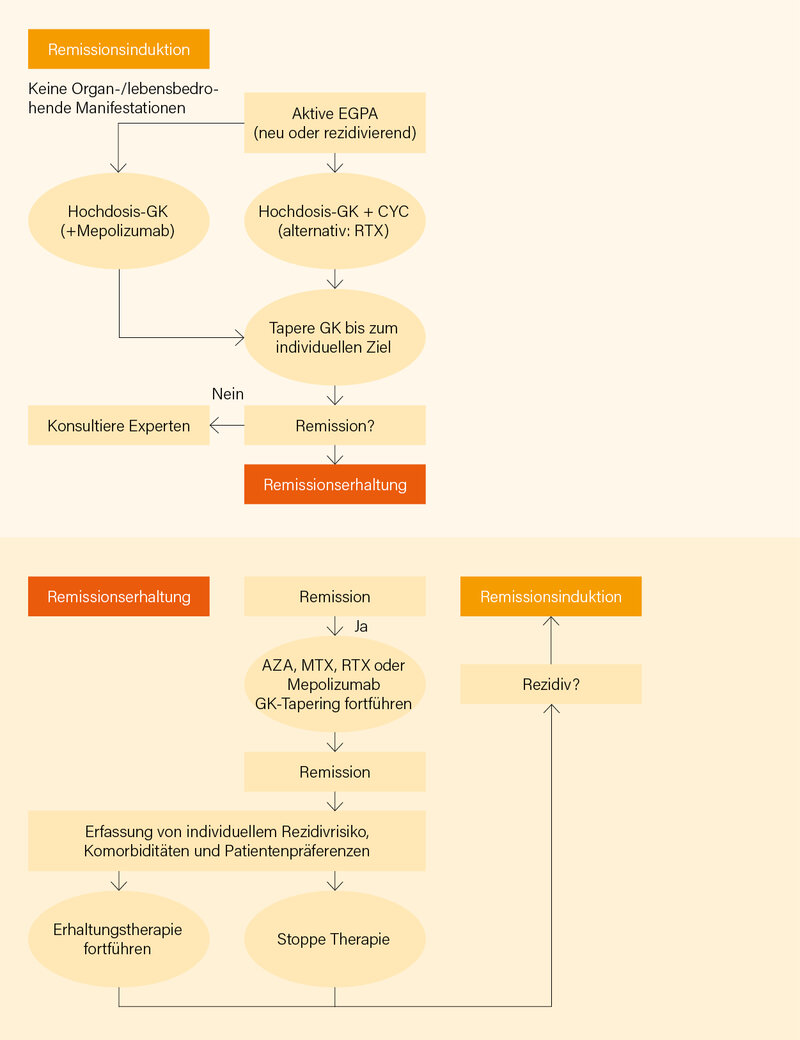
Unverändert blieb Empfehlung (15): Beim Management von AAV-Patienten wird empfohlen, dass eine strukturierte klinische Untersuchung, eher als eine alleinige ANCA- und/oder CD19+ B-Zell-Testung, die Entscheidung für einen Therapiewechsel leiten sollte. Gleiches gilt für (16): Bei AAV-Patienten mit RTX-Therapie wird die Messung der Serum-Immunglobulin-Konzentrationen vor jedem RTX-Zyklus zur Entdeckung einer sekundären Immundefizienz empfohlen. Aufgrund neuer Studiendaten revidiert wurde Empfehlung (17): Für AAV-Patienten, die RTX, CYC und/oder Hochdosis-GK erhalten, wird zur Prophylaxe gegen Pneumocystis jirovecii-Pneumonie (PJP) oder andere Infektionen der Einsatz von Trimethoprim/Sulfamethoxazol empfohlen. Wie üblich wurden Therapiealgorithmen, separat für GPA/MPA (Abb. 1) und EGPA (Abb. 2), entwickelt.
Quelle: EULAR Recommendations Session, 1. Juni 2022